
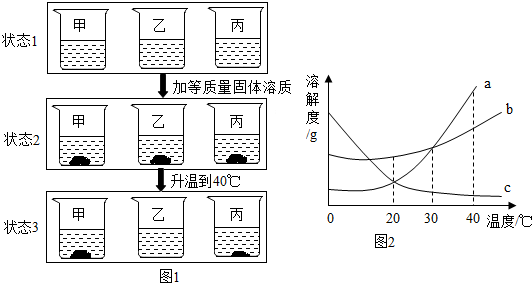
分析 根据题目信息和溶解度曲线可知:a、b两种固体物质的溶解度,都是随温度升高而增大,而c的溶解度随温度的升高而减少;三种物质的溶解度关系为b>a>c时的温度为t℃时,则t的取值范围是:20℃<t<30℃;由图1和图2可知:烧杯甲里是c物质的溶液,因为升温后c变多了;烧杯乙里是a物质的溶液,因为升温后,a全部溶解.若将40℃时的三物质的饱和溶液分别降温到20℃时,则三种溶液中的溶质的质量分数由大到小的顺序是:b>a>c;40℃时,烧杯b里的溶液中溶剂最少,因为在原温度时,b的溶解度最大,因此溶剂最少,升温后,溶剂没有改变;各种状态下,各烧杯(甲、乙、丙)里的溶液中溶质质量分数的比较一定正确的是:乙(状态1)>甲(状态3),甲(状态1)=乙(状态2).
解答 解:(1)由溶解度曲线可知,三种物质的溶解度关系为b>a>c时的温度为t℃时,则t的取值范围是:20℃<t<30℃;故答案为:20℃<t<30℃;
(2)由图1和图2可知:烧杯甲里是c物质的溶液,因为升温后c变多了;烧杯乙里是a物质的溶液,因为升温后,a全部溶解;故答案为:c;a;
(3)若将40℃时的三物质的饱和溶液分别降温到20℃时,则三种溶液中的溶质的质量分数由大到小的顺序是:b>a>c;故答案为:b>a>c
(4)40℃时,烧杯b里的溶液中溶剂最少,因为在原温度时,b的溶解度最大,因此溶剂最少,升温后,溶剂没有改变;故答案为:b
(5)各种状态下,各烧杯(甲、乙、丙)里的溶液中溶质质量分数的比较一定正确的是:乙(状态1)>甲(状态3),甲(状态1)=乙(状态2);故答案为:BC;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液升温和降温后溶质质量分数的变化等,本考点主要出现在选择题和填空题中.


科目:初中化学 来源: 题型:解答题
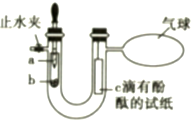 某同学在学完《分子和原子》后,对教材中的实验进行了如图所示的改进:
某同学在学完《分子和原子》后,对教材中的实验进行了如图所示的改进:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 该温度下,固体物质的溶解度可能是30g | |
| B. | 溶液丙再蒸发10g水,析出晶体质量可能大于3g | |
| C. | 溶液乙一定是不饱和溶液 | |
| D. | 溶液乙和溶液丙中的溶质质量分数可能相等 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
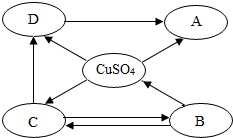 构建知识网络是学习化学的重要方法,如图是不同物质相互转化关系图.其中A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,C为红色粉末.“→”表示一种物质一步转化成另一种物质(部分反应物、生成物及反应条件未标出),请回答问题:
构建知识网络是学习化学的重要方法,如图是不同物质相互转化关系图.其中A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,C为红色粉末.“→”表示一种物质一步转化成另一种物质(部分反应物、生成物及反应条件未标出),请回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 化学式 | A | B | C | D |
| 反应前质量(g) | 28 | 102 | 4 | 4 |
| 反应后质量(g) | 0 | 6 | 92 | 未知 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com