
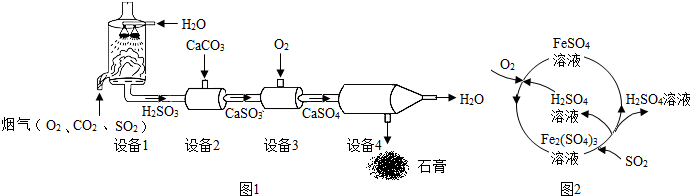
分析 (1)根据二氧化硫和水反应生成亚硫酸,将烟气中的SO2直接排放到空气中,可能会导致酸雨进行分析;
(2)根据碳酸钙和亚硫酸反应会生成亚硫酸钙、水和二氧化碳进行分析;
(3)根据亚硫酸钙和氧气反应生成硫酸钙,反应前后各元素的化合价进行分析;
(4)根据质量守恒的和流程中各物质参与的反应进行分析.
解答 解:(1)二氧化硫和水反应生成亚硫酸,化学方程式为:SO2+H2O=H2SO3,将烟气中的SO2直接排放到空气中,可能会导致酸雨;
(2)碳酸钙和亚硫酸反应会生成亚硫酸钙、水和二氧化碳,所以设备2中,加入CaCO3的目的是将H2SO3转化为CaSO3;
(3)亚硫酸钙和氧气反应生成硫酸钙,化学方程式为:2CaSO3+O2=2CaSO4,反应中化合价升高的元素是S;
(4)①生成物质中2个铁原子,4个硫原子,16个氢原子,8个氧原子,反应物中2个铁原子,4个硫原子,14个氧原子,所以空格处是H2O;
②通过分析反应流程可知,硫酸、硫酸亚铁既是反应物,也是生成物,所以该流程中可循环利用的物质是H2SO4和FeSO4.
故答案为:(1)SO2+H2O=H2SO3,形成酸雨;
(2)CaSO3;
(3)2CaSO3+O2=2CaSO4,S;
(4)①H2O,②H2SO4和FeSO4.
点评 本题考查了燃料脱硫的原理等,题中难度中等,注意化学方程式的书写,为该题的易错点和难点.注意流程分析和设计方法和理解是解答的关键.


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:初中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ②①④③⑤⑥ | C. | ②①③④⑤⑥ | D. | ②③④①⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲状腺肿大可能是缺铁所致 | |
| B. | 霉变的花生米洗净后仍可正常食用 | |
| C. | 可用结晶的方法提纯混有少量氯化钠的硝酸钾 | |
| D. | 铅、金、钛属于金属元素,硫、氮、汞属于非金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧化反应一定是化合反应 | |
| B. | 复分解反应中各元素的化合价一定不变 | |
| C. | 置换反应一定有单质生成 | |
| D. | 有盐和水生成的反应不一定是中和反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一定是烧碱溶液 | B. | 一定是酸溶液 | C. | 可能是中性溶液 | D. | 一定是盐溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | ②没有气泡生成 | 猜想1正确 |
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量③氯化钡溶液(或氯化钙溶液). | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 2.过滤、取少量滤液加入 ④无色酚酞试液 | ⑤试液变红 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com