
| A. | 该纯净物中含有C、H元素,不含O元素 | |
| B. | 该反应中O2和CO2的质量比为14:11 | |
| C. | 该反应中O2和H2O的分子数之比为7:6 | |
| D. | 该纯净物中C、H原子的个数比为1:4 |
分析 根据质量守恒定律的含义(即六不变)中的“元素的种类不变”可知,生成物所含的碳、氢、氧三种元素中的碳元素和氢元素一定来自于纯净物,至于氧元素可能全部来自于氧气,也可能部分来自于氧气,另一部分则来自于3g物质,可根据元素的质量不变进行判断;根据生成物CO2和H2O中C、H元素质量,让碳氢元素的质量分别除以各自的相对原子质量再相比,就可以得到该物质中碳氢两元素的原子个数比.
解答 解:A、根据质量守恒定律可知,化学反应前后元素的种类保持不变;说明该物质一定含有氢元素和碳元素,可能含有氧元素;
又因为:二氧化碳中碳元素的质量等于8.8g×$\frac{12}{44}$=2.4g,水中氢元素的质量等于5.4g×$\frac{2}{18}$=0.6g,
因此氢元素和碳元素的质量之和是2.4g+0.6g═3.0g,说明该物质仅含有碳元素和氢元素,故说法正确.
B、根据质量守恒定律可知,参加反应的氧气的质量为8.8g+5.4g-3g=11.2g,则该反应中O2和CO2的质量比为11.2g:8.8g=14:11,故说法正确;
C、反应中O2和H2O的分子数之比为$\frac{11.2g}{32}$:$\frac{5.4g}{18}$=7:6,故说法正确;
D、该纯净物中C、H原子的个数比为$\frac{2.4g}{12}$:$\frac{0.6g}{1}$=1:3,故错误.
故选:D.
点评 本题主要考查有关化学式的计算,难度稍大.关键是找到确定该物质的元素组成、元素质量和原子个数比的方法.


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:初中化学 来源: 题型:实验探究题
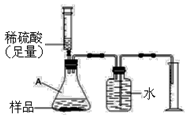 侯德榜是我国著名的化学家.由他发明的侯氏制碱法制得的纯碱中含有少量氯化钠杂质.某化学兴趣小组的同学为了测定该厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的质量分数不低于99.2%),设计了如下两种实验方案
侯德榜是我国著名的化学家.由他发明的侯氏制碱法制得的纯碱中含有少量氯化钠杂质.某化学兴趣小组的同学为了测定该厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的质量分数不低于99.2%),设计了如下两种实验方案查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 起始原料是①③ | B. | 起始原料是②⑥ | C. | 最终产品是⑤⑥ | D. | 最终产品是③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镆属于金属元素 | B. | 镆铘剑含有镆元素 | ||
| C. | 镆原子的质子数为115 | D. | 镆铘剑由合金铸造 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
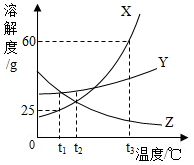 如图所示为X、Y、Z三种固体物质(不含结晶水)的溶解度曲线,请回答下列问题:
如图所示为X、Y、Z三种固体物质(不含结晶水)的溶解度曲线,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤液中的溶质一定含有硝酸铜 | B. | 滤液中溶质一定不含硝酸银 | ||
| C. | 滤渣中可能含有银和锌 | D. | 滤渣中一定没有铜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com