
| A. | 反应速率不变 | B. | 反应速率加快,生成氧气质量增加 | ||
| C. | 生成氧气质量不变 | D. | 反应速率加快,生成氧气质量不变 |
分析 高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰和氧气,二氧化锰可作为氯酸钾制取氧气的催化剂,加快化学反应速率;据此进行分析判断.
解答 解:A、生成的二氧化锰可作氯酸钾反应的催化剂,可加快化学反应速率,所以反应速率加快,故选项说法错误;
B、高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰和氧气,生成的二氧化锰可作氯酸钾反应的催化剂,可加快化学反应速率;生成氧气的质量与单纯加热氯酸钾相比,质量增加,故选项说法正确;
C、生成的二氧化锰可作氯酸钾反应的催化剂,可加快化学反应速率,所以反应速率加快,生成氧气质量增加,故选项说法错误;
D、高锰酸钾分解可生成氧气,生成氧气的质量与单纯加热氯酸钾相比,质量要增加,故选项说法错误;
故选B.
点评 本题难度不大,掌握高锰酸钾和氯酸钾制取氧气的反应原理及二氧化锰在氯酸钾反应中的作用并能灵活运用是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 非吸烟者受到被动吸烟的危害,是因为分子在不断地运动 | |
| B. | 氧气加压后变成液氧,是因为分子间的间隔变小 | |
| C. | 1滴水中含有约1.67×1021个水分子,说明水分子很小 | |
| D. | 水受热蒸发后变成水蒸气,说明水分子的化学性质发生了改变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
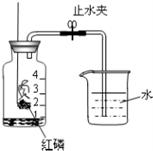 小林设计了测定空气中氧气含量的实验,实验裝置如图所示.
小林设计了测定空气中氧气含量的实验,实验裝置如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
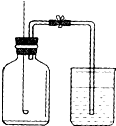 某同学用如图装置测定空气中氧气的体积分数.请你填写有关空格,并与同学交流.
某同学用如图装置测定空气中氧气的体积分数.请你填写有关空格,并与同学交流.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2CO3、K2SO4、HCl | B. | FeCl3、NaNO3、NaOH | ||
| C. | Ca(OH)2、NaCl、HCl | D. | Na2SO4、NaNO3、H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com