
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:初中化学 来源: 题型:实验探究题
 为了测定空气中氧气的含量,小华设计了如下方案:选用实际溶剂为40ml的直玻璃管作反应容器,将过量的白磷放入试管,用橡皮塞紧直玻璃管,通过导管与实际容积为60mL的且润滑性很好的针筒注射器组成如图所示的实验装置.假设此装置能按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:
为了测定空气中氧气的含量,小华设计了如下方案:选用实际溶剂为40ml的直玻璃管作反应容器,将过量的白磷放入试管,用橡皮塞紧直玻璃管,通过导管与实际容积为60mL的且润滑性很好的针筒注射器组成如图所示的实验装置.假设此装置能按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
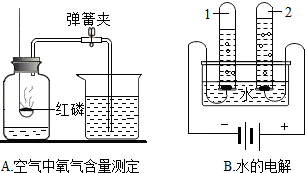 氧气和水是我们身边重要的物质.A、B都是研究物质组成和性质的实验.
氧气和水是我们身边重要的物质.A、B都是研究物质组成和性质的实验.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
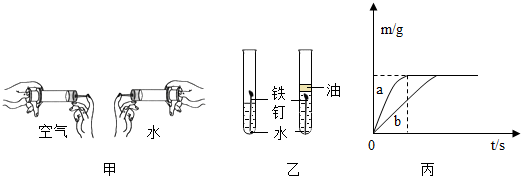
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气加压后变成液氧,是因为分子间的间隔变小 | |
| B. | 水通电生成氢气和氧气,因为水分子中含有氢分子和氧分子 | |
| C. | NaOH和Ca(OH)2化学性质相似,因为在水中解离出的阴离子都是OH- | |
| D. | 蔗糖溶液是混合物,因为蔗糖溶液是由不同种分子构成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
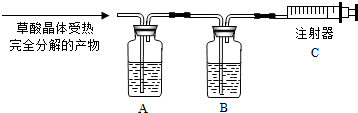
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
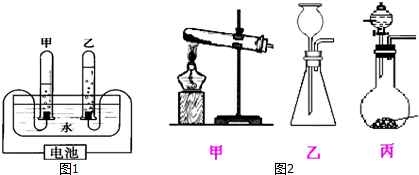
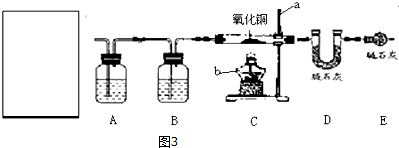
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 反应过程中有气泡产生 | |
| B. | 生成MgCl2的质量为9.5g | |
| C. | 反应后溶液中的溶质只有MgCl2 | |
| D. | 所用稀盐酸中溶质的质量分数为14.6% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com