
【题目】根据下列实验装置图,回答下列有关问题:

(1)图中标有①的仪器名称是_______。
(2)如果用A装置制取二氧化碳,检查气密性后在锥形瓶内加入的固体物质是________,写出用A装置制取二氧化碳的化学方程式:_______________。
(3)用一定质量的KClO3和MnO2制取O2,用排水法收集并测量产生O2的体积,则应该让____导管与c连接。所测定的O2体积比理论计算值小,可能的原因是________(填序号)。
①部分氧气溶于水 ②集气瓶中有空气 ③氯酸钾未完全分解
(4)用实验证明氢氧化钙溶液与稀盐酸能发生反应,氢氧化钠溶液与二氧化碳也能发生反应。如图所示进行实验(装置气密性良好,实验前活塞和弹簧夹K处于关闭状态)。
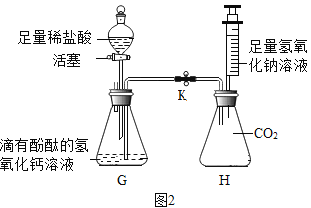
实验一:证明氢氧化钙溶液与稀盐酸发生反应
打开分液漏斗的活塞,使稀盐酸逐滴滴加入G锥形瓶中,观察到_______的现象时,关闭活塞,证明氢氧化钙溶液与稀盐酸发生反应。
实验二:证明氢氧化钠与二氧化碳反应
将注射器中的氢氧化钠溶液推入H锥形瓶中,过一段时间后,打开弹簧夹K,观察到__________的现象并且溶液呈红色,证明氢氧化钠溶液与二氧化碳确实发生了反应。请写出二氧化碳与氢氧化钠溶液反应的化学方程式是_______。锥形瓶H中溶液最后呈红色_________(填“能”或“不能”)证明氢氧化钠有剩余。
【答案】长颈漏斗 石灰石或大理石 2HCl+CaCO3=CaCl2+H2O+CO2![]() a ①③ 红色溶液变为无色 G中溶液倒流进H中产生白色沉淀 2NaOH+CO2=Na2CO3+H2O 不能
a ①③ 红色溶液变为无色 G中溶液倒流进H中产生白色沉淀 2NaOH+CO2=Na2CO3+H2O 不能
【解析】
(1)由图可知,①的仪器名称是长颈漏斗,故填写:长颈漏斗;
(2)制取二氧化碳的固体是石灰石或大理石,故填写:石灰石或大理石;
石灰石与稀盐酸反应生成氯化钙、水和二氧化碳,故填写:2HCl+CaCO3=CaCl2+H2O+CO2![]() ;
;
(3)用排水法收集氧气,导管应放在集气瓶口,故b为进气口,a为出气口,故填写:a;
所测定的O2体积比理论计算值小,可能的原因是部分氧气溶于水和氯酸钾未完全分解,本实验用排水法收集氧气,如图所示,集气瓶中装满水,没有空气,不可能导致所测氧气体积偏小,故填写:①③;
(4)酚酞遇碱性的氢氧化钙会变红,当氢氧化钙与稀盐酸完全反应完,溶液为中性,酚酞会变为无色,故填写:红色溶液变为无色;
氢氧化钠溶液注入二氧化碳,二氧化碳被反应吸收,压强变小,打开弹簧夹K,G中溶液倒流进H,倒流进来的氢氧化钙与反应生成的碳酸钠反应生成了白色沉淀,同时,溶液也变红,故填写:G中溶液倒流进H中产生白色沉淀;
氢氧化钠与二氧化碳反应生成碳酸钠和水,故填写:2NaOH+CO2=Na2CO3+H2O;
锥形瓶H中溶液最后呈红色不能证明氢氧化钠有剩余,因为氢氧化钠与二氧化碳反应生成的碳酸钠也可以使酚酞变红,当碳酸钠剩余时,也可以使溶液变红,故填写:不能。


科目:初中化学 来源: 题型:
【题目】下列化学用语表达正确的是 :
A.H2中的“2”表示2个氢原子
B.硫酸钠溶液中所含的酸根离子:SO42+
C.过氧化氢中氢、氧元素的化合价:![]()
D.铁锈和盐酸反应的化学方程式:Fe2O3+6HCl=2FeCl2+3H2O
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是五种物质的部分相互转化关系图,其中A、B、C、D分别是初中化学常见的不同类别的化合物(酸、碱、盐和氧化物),C为胃酸的主要成分,D是一种红棕色粉末(“→”表示反应转化关系,“—”表示相互之间能反应,部分反应物、生成物以及反应条件省略)。请回答下列问题:

(1)C的化学式是__________,D的名称是_______。
(2)工业上,能使D转化为铁的物质是______。
(3)若A是碱,则B可能是_________________(写化学式)。
(4)若A是钠盐,写出B与C反应的化学方程式_______,该反应的基本类型是______反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶化肥的标签已脱落,只知道它是NH4Cl、(NH4)2SO4、NH4HCO3和尿素[CO(NH2)2]中的一种。请你完成以下探究:
(猜想)猜想①:该化肥是NH4Cl,
猜想②:该化肥是 ,
猜想③:该化肥是NH4HCO3,
猜想④:该化肥是尿素。
(实验探究)
(1)取少量样品在研钵中与熟石灰研磨,有刺激性气味的气体放出,证明猜想 不成立;写出其中一种化肥发生该反应的化学方程式: 。
(2)如(图1),另取少量样品于试管中,滴加适量水振荡,再选(图2)中 溶液滴入试管中,若无气泡放出,则猜想 不成立。
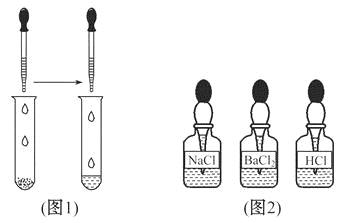
(3)在步骤(2)的试管中再滴入(图2)中的 溶液,若 ,则猜想①成立;若 ,则猜想②成立,其反应的化学方程式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将一定质量的MgO和CaO的混合物加入到100g溶质质量分数为14.6%的稀盐酸中,恰好完全反应,反应后将所得溶液蒸干得到20.6g固体.下列说法正确的是
A.原混合物质量为9.6gB.反应后所得溶液质量为114.6g
C.反应生成水的质量为3.6gD.与MgO和与CaO反应的HCl质量比可能为1:3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲醛(CH2O)是无色气体,有刺激气味,易溶于水,其水溶液的浓度为30%-40%称为甲醛水,俗称福尔马林。下列说法正确的有( )
①甲醛的相对分子质量为30
②甲醛分子中含有4种元素
③甲醛水有刺激性气味,说明甲醛分子在不断运动,水分子没有运动
④无论甲醛水质量,浓度为多少,其中氢元素、氧元素的质量比都为18
⑤若甲醛水中碳元素质量分数为13.6%,则其中氧元素的质量分数为76.8%
A.2个B.3个C.4个D.5个
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示是实验室电解水的装置图,请回答下列问题:
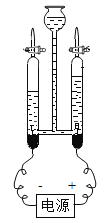
(1)接通直流电源段时间后,在两个电极观察到的现象是________________。
(2)切断装置中的电源,把燃着的木条放在________极玻璃管尖嘴口处,发现_____________,说明生成的气体是氢气。
(3)电解水的文字表达式为:![]() 通过该实验得出的结论:水是由______________组成的;在化学反应前后,________________的种类没有改变。
通过该实验得出的结论:水是由______________组成的;在化学反应前后,________________的种类没有改变。
(4)电解水的基本反应类型是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水在实验室中应用也很广泛,水在化学实验中的作用不可忽视,图中五个实验分别用到水,请回答:
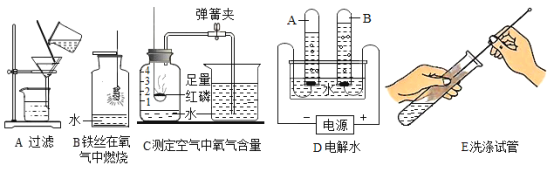
①实验A中玻璃棒的作用是_____________________;
②实验B中水的作用是_____________________;
③实验C中通过烧杯中的水进入集气瓶中的体积可得出氧气约占空气体积的_________________结论;
④实验D中,电解水时,当其中一电极产生5mL气体时,另一电极产生的气体可能_________mL;
⑤实验F中,试管洗涤干净的标准是_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com