
����Ŀ����ͼ��ľ̿��ԭ����ͭ��̽��ʵ��װ�ã�
��������⡿ľ̿��ԭ����ͭ����ʲô���壿
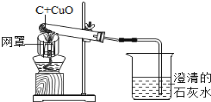
��������롿�����������������������CO����CO2����________________��
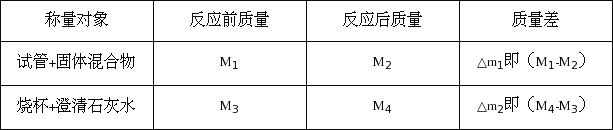
����Ʒ�����ʵ��ǰ��ֱ���Թܺ��ձ�������ʽ��г���������������£�
��1������m2=0��˵����Ӧ���������岻�ܱ�����ʯ��ˮ���գ������_____________������
��2�����������ȷ�������ϡ�m1���m2�Ĺ�ϵ�ǣ���m1___________��m2�����������������=������
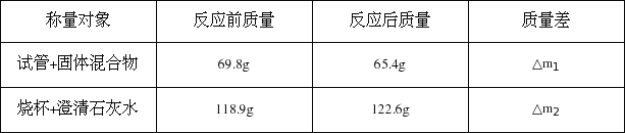
��ʵ�鲢��¼��ʵ��õ����������±���
������ʵ�����ݷ��������Ӧ���Dz���_____________������
ͬѧ�Ƕ�CO������ԭ�������
��ԭ��һ��ľ̿������ͭ�ڸ���������ֱ�ӷ�����������CO����Ӧ����ʽΪ
��ԭ�����ľ̿������ͭ�ڸ��������·�Ӧ�е�һ�ֲ���ͷ�Ӧ��ľ̿�ַ����˻�ѧ��Ӧ��������CO����Ӧ����ʽΪ_____________________
����˼�����ۡ�����������֪����ľ̿��ԭ����ͭ����CO2���壬��Ӧ��ѧ����ʽΪ��___________��
����ʵ������������ʾ��һ�£��������ԭ����ͬѧ������з��������к�������_____________��
A��װ��©��
B�����ɵ�CO2�����������C��Ӧ������CO
C������ʯ��ˮ����CO2Ч������
D��װ���ڻ���CO2����δ�����գ�
������������6��̼��һ������������ͭǡ����ȫ��Ӧ�����ɵ�������ȫ��������ʯ��ˮ���գ��ɵõ��������ٿˣ�
���𰸡���������롿��CO��CO2
����Ʒ�������1������2��=
��ʵ�鲢��¼��������
ԭ��һ2CuO+C![]() 2Cu+CO2����
2Cu+CO2����
ԭ���CO2+C![]() 2CO
2CO
����˼�����ۡ�2CuO+C![]() 2Cu+CO2����BCD
2Cu+CO2����BCD
������������:50 g
��������
������������롿�۷�Ӧǰ��Ԫ�ص�����䣬�ʿ�����CO��CO2�Ļ�����塣����Ʒ�������1������ʯ��ˮ�����ն�����̼����������һ����̼���ʡ�m2=0��˵������ٳ������������ڳ���������װ�ò���������̼���������ڳ���ʯ��ˮ���ն�����̼������������m1=��m2
��ʵ�鲢��¼����m1=69.8g-65.4g=4.4g����m2=122.6g-118.9g=3.7g��4.4g��3.7g������۳�����
��ľ̿������ͭ�ڸ���������ֱ�ӷ�����������CO2����Ļ�ѧ����ʽ�ǣ�
��2CuO+C![]() 2Cu+CO2������ԭ�����ľ̿������ͭ�ڸ��������·�Ӧ���ɵ�CO2�ͷ�Ӧ��ľ̿������ѧ��Ӧ�Ļ�ѧ����ʽ�ǣ�CO2+C
2Cu+CO2������ԭ�����ľ̿������ͭ�ڸ��������·�Ӧ���ɵ�CO2�ͷ�Ӧ��ľ̿������ѧ��Ӧ�Ļ�ѧ����ʽ�ǣ�CO2+C![]() 2CO��
2CO��
����˼�����ۡ�����������֪����ľ̿��ԭ����ͭ����CO2���壬����ʵ������������ʾ��һ�£������ԭ�������ɵ�CO2�����������C��Ӧ������CO������ʯ��ˮ����CO2Ч�����á�װ���ڻ���CO2����δ�����գ���ѡB��C��D��������������C��CO2��CaCO3֮��Ķ�Ӧ��ϵ�ǣ�
C-----CO2--------CaCO3����õ�������������X����C-----CO2--------CaCO3
12 100
6�� X
12/100=6��/ X ���X=50�ˡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ʵ��Ϊ������ѧ�û�ѧҪ����ʵ�顣
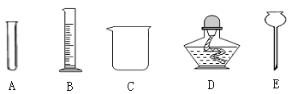
��1��ʵ��ǰҪ��Ϥʵ��������������������ͼ�dz��л�ѧʵ���ҳ��õ��������������мȿ�����Ϊ��Ӧ�������ֿ����ڼ���ʱʹ�õ���__________������ţ�������E��������___________��
��2����ѧʵ��Ҫ�ϸ���Ҫ����У��ں�������д���´��������ɵĺ����
��ʵ������ʣ��ҩƷ�Ż�ԭƿ_______________��
������Ͳ��ȡ20mLˮ���Ӷ�������ȡˮ�������_____���ƫ��ƫС������
��3��ʵ��ʱҪ����۲�ʵ������ѧ������ó���ȷ���ۡ��ܴ���ͼ��ʾʵ�鼰����ó��Ľ�����___________������ţ���

A.������̼�ܶȱȿ����� B.������̼����ȼ��
C.������̼��֧��ȼ�� D.����ȼ�ղ����к��ж�����̼
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ⲻ�ȶ�����Ȼ�ֽ⣬���õĹ���������Һ�������ʵ������������С��ij��ȤС��Ϊ�ⶨʵ������һƿ���õĹ���������Һ�����ʵ���������������ʵ�顣������������ͼ9��ʾ��
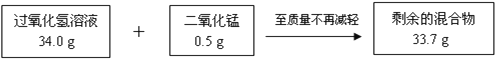
(1)���������غ㶨�ɣ���Ӧ��������������Ϊ_______��
(2)����ù���������Һ�����ʵ���������Ϊ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������ҩ������������ͭ��ȼ��ʱ������ɫ����,�������·�Ӧ:2Cu(NO3)2 ![]() 2CuO + O2�� + 4X���������й�˵���������( )
2CuO + O2�� + 4X���������й�˵���������( )
A. ���������غ㶨�ɿ�֪X�Ļ�ѧʽΪNO2
B. �÷�Ӧ�Ļ�����Ӧ����Ϊ�ֽⷴӦ
C. Cu(NO3)2��ͭԪ�صĻ��ϼ�Ϊ+1
D. ������CuO����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��һ����ʵ��Ϊ������ѧ�ơ�������ͼ,�ش����⡣
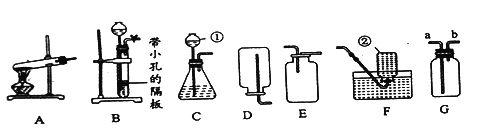
��1��д�������ָ����������:��________________����_______________��
��2������װ��ͼ�����������ԵĴ���,�����ҳ�����ĵط����Ѹ����Ľ���������к����ϣ���________________����_______________��
����װ�øĽ���������ش��������⣬
��3��С����ʵ������������غ���һ�ֹ�����ȡ����,��ѡ������װ���е�A��_____(����ĸ)������װС����ʵ������ѡ��Cװ����Ϊ�����ķ���װ��.�����ǵ�ʵ���ж��õ���һ����ͬ�Ĺ���ҩƷ��_____________(�ѧʽ),��������Ӧ������__________���á�����д��С����ȡ�����Ļ�ѧ��Ӧ����ʽ:_____________________________��
��4��ʵ����ѡ��C��Eװ�û�������ȡ��������_______���ѧʽ����д��ʵ������ȡ������Ļ�ѧ����ʽ��__________________________________��
��5��װ��B��C������������ȡ(4)�е����壬�Ƚ�������װ�õIJ�ͬ��ָ��Bװ�õ�һ��ͻ���ŵ�____________________________________��
��6����һ��ͬѧ����Gװ���ռ�![]() ,��
,��![]() Ӧ�ӵ��ܿ�____________ͨ��.
Ӧ�ӵ��ܿ�____________ͨ��.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����д�����з�Ӧ�Ļ�ѧ����ʽ��
��1��þ���ڿ�����ȼ�գ� ______________________________________________��
��2����������غͶ������̻���___________________________________��
��3�������ڿ�����ȼ�գ�_______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������벻��������
(1)�ڵؿ��ﺬ�����Ľ���Ԫ����ǽ���Ԫ����ɵĻ�������(�ѧʽ)__��
(2)����ͭ��Ʒ����;�У����ý��������Ե���__(����ĸ)��

(3)ͭ�ڳ�ʪ�Ŀ�����Ҳ�����������γ�ͭ�̣�ͭ�̵���Ҫ�ɷ�Ϊ Cu2(OH)2CO3���ɴ˿����Ʋ⣺ͭ�������������У����뷴Ӧ��������ͭ��������ˮ��__��
(4)�������ֽ��������֡�ʹ�õ��Ⱥ�˳������Ϊ��ͭ�����������������ģ��ʹ�õ��Ⱥ�˳���__(����ĸ)��ϵ���
A���ؿ��н���Ԫ�صĺ��� B�������ĵ����� C�������Ļ��
(5)������ÿ����Ϊ��������ϵ�����Ʒռ���ܲ�����20%��40%������������Դ������������д��һ����ֹ������Ĵ�ʩ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��þ��һ������ɫ�н�������Ľ���������ʵ�����ó���þ����������һ��Һ�ɫ�ġ����¡���
��1������������⣩���Һ�ɫ��������ʲô�����أ�
���������ϣ���ˮ����ͭ�ǰ�ɫ�Ĺ��壬��ˮ������ɫ��
�����룩����1���Һ�ɫ���ʿ�����MgO ����2���Һ�ɫ���ʿ�����Mg2��OH��2CO3
����3���Һ�ɫ���ʿ�����Mg��OH��2
���������У��϶����������Dz���1��������__________________________________��
��2������ʵ��̽����ȡ�Һ�ɫ���ʰ��������̽���ʵ�飺
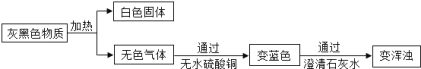
���������ۣ�
����ˮ����ͭ����ɫ��˵���Һ�ɫ���ʼ��ȷֽ������___________��
�ڳ���ʯ��ˮ����ǣ�˵���Һ�ɫ������Ȳ�����____________����˲���______������ ��д������ʯ��ˮ����ǵķ�Ӧ��ѧ����ʽ_______________��
�ۻҺ�ɫ���ʼ��ȷ�����Ӧ�Ļ�ѧ����ʽΪ___________________________________��
��þ����ĻҺ�ɫ���ʣ���þ������е�O2��__________________������Ӧ���ɵġ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ҫ�Ľ������ϣ��ڹ�ũҵ������������Ӧ�÷dz��㷺��
��������Ӧ��
��1����������Ʒ������������������йص��� ������ĸ����ͬ����
A����ǯ B������ C������
��2�������צ�-Fe�ۡ���������ʳƷ���ʣ���֮Ϊ��˫����������Ϊ�������տ����е� ��
��������ұ��
��ҵ������ԭ���Ǹ�������CO����ԭ�����������������л�ԭ��������ش��������⣺
��1��д���Գ�����Ϊԭ�ϣ��ڸ����������Ļ�ѧ����ʽ�� ��
��2����¯�����У���̿�����ó��˿�������һ����̼�⣬���� ��
����ʵ��̽������ԭ��
ij��ѧ��ȤС����ʵ������ģ�ҵ������ԭ������̽��CO��Fe2O3��Ӧ��IJ��
ͨ����������֪���������ᣨH2C2O4��������Ũ�����ϼ��Ȼ����һ����̼����Ӧ����ʽΪ��H2C2O4 ![]() CO��+ CO2��+ H2O��
CO��+ CO2��+ H2O��
��NaOH��Һ�������ն�����̼����Ӧ����ʽΪ��2NaOH+CO2=Na2CO3+H2O
�������£�Ca(OH)2����ˮ��
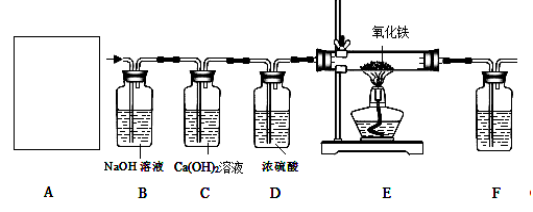
�������������ͼ��ʵ��װ�ã����װ�ûش��������⣺
��1��ͼA���ù�������Ũ������ȡCO�ķ�Ӧװ�ã�����ΪӦѡ����ͼ�е� ����װ�ñ�ţ���
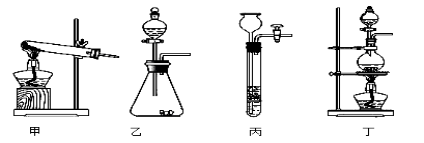
��2��ͼ��װ��C��D�����÷ֱ��� �� ��
��3��Ϊ��֤���������ж�����̼��װ��F�е��Լ�Ӧ���������� �����Լ����ƣ�����Ӧ�Ļ�ѧ����ʽΪ ��
��4����װ�������һ������ȱ�ݣ�����Ϊ�� ��
��5��ʵ��ʱȷ��ȡһ������������Fe2O3���尴��ͼ����ʵ�飬��E�й���ȫ����ں���ͨ��COֱ����������ȴ�����õ���ɫ�Ĺ�����뵽������ϡ���ᣬ���ֹ���ȫ���ܽ⣬�������ݲ�����
�������ϣ�a. ������������������ϡ�����о���ȫ���ܽ⡣
b. Fe2O3��CO��Ӧ�Ĺ������������������£�
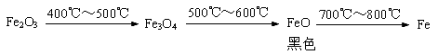
���ݡ������ݡ����룬��ɫ��ĩ�����ǣ��� Fe3O4 ���� �� ��
��6���������� �õ�����ƽ�����ò����������£�
���������� | �����ܼ����й�������� | װ��F���������ʵ������� | |
��Ӧǰ | 28.20 g | 33.00 g | 300.0 g |
��Ӧ�� | 32.84 g | 300.4 g |
�����������ݣ�������Fe2O3��������Ϊ g����ѡ����Ч�����ݣ��ƶϳ���Ӧ���ɫ����ijɷ֡���д��������̣� ��
�����ƶϽ����д����ʵ���в������ڷ����Ļ�ѧ��Ӧ����ʽ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com