
| A. | 常用带火星的木条来检验空气中的O2 | |
| B. | 硫在O2里燃烧产生明亮的蓝紫色火焰 | |
| C. | 工业上将空气液化后再进行分离来制取O2 | |
| D. | 鱼类可以在水中呼吸说明氧气易溶于水 |
分析 A、根据氧气的检验方法分析;
B、根据硫在氧气中燃烧的现象分析;
C、根据工业制氧气的方法分析;
D、根据氧气溶解性分析.
解答 解:A、常用带火星的木条来检验纯O2,空气中的氧气不能使带火星的木条复燃,故错误;
B、硫在氧气中燃烧的现象:发出明亮的蓝紫色火焰,放出热量,生成一种刺激性气味的气体,故正确;
C、工业制氧气的方法是分离液态空气法,先将空气液化,利用液态氮的沸点比液态氧的沸点低的原理将二者分离来制取氧气,故正确;
D、鱼类能在水中生存,说明了水中溶有一定量的氧气,不能说明氧气易溶于水,氧气的溶解性是不易溶于水.故错误;
故选:AD.
点评 本题考查学生对氧气制取、性质等知识的理解与在解题中应用的能力.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论或总结 | ||
| 结论 | 总结 | |||
| 实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是反应速率慢. | 二氧化锰是过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | 二氧化锰加入水中不产生氧气 | |
| 实验三 | 向盛有5mL5%过氧化氢溶液的试管中加入二氧化锰,伸入带火星的木条 | 有大量气泡产生,带火星的木条迅速复燃 | 二氧化锰能加快过氧化氢的分解反应的化学表达式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在空气中,不燃烧的物质,在氧气里也一定不燃烧 | |
| B. | 钢铁生锈,食物腐烂都是缓慢氧化的结果 | |
| C. | 不用催化剂,加热氯酸钾就不会分解出氧气 | |
| D. | 使用催化剂可以使氯酸钾分解出更多的氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 试管:同学们不爱惜我,我被摔碎了 | |
| B. | 铁钉:好难受啊,我在潮湿的空气中生锈了 | |
| C. | 灯泡:我通电后发光了,给学生带来光明 | |
| D. | 饼干:我在空气中变软了 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
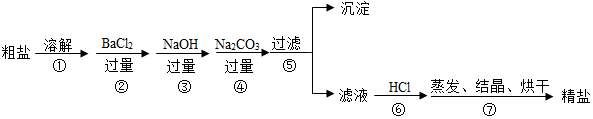
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com