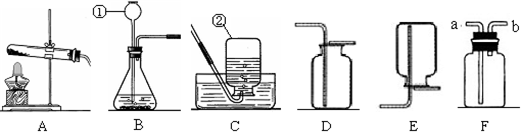
解:(1)图中①是用于添加液体的长颈漏斗,②是集气瓶.
(2)H
2、CO
2、O
2可用上图中的同一种装置来制取,由于三种气体均可在不加热条件下进行,所以可以用的装置B.其中有一种气体可用A、B两种装置制取,该气体应该为氧气,但是由于A中没有棉花团,所以一般不写高锰酸钾的分解的反应.(3)若用装置D收集某气体,由于D装置是向上排空气法收集,所以该气体一定是密度大于空气,且不能和空气中任一组分发生反应,所以气体可以为氧气或者二氧化碳.
(4)制取二氧化碳要用大理石与稀盐酸反应,由于二氧化碳密度比空气大,所以收集装置为D;因二氧化碳不支持燃烧,验满的方法是将燃着的木条放在集气瓶口,木条熄灭说明已满.
(5)用加热氯化铵和消石灰的固体混合物制取氨气,由于反应是固体加热条件下完成的,所以发生装置为A.由于氨气的密度小于空气,所以当用F装置来收集时,应该选用向下排空气法,即短进长出,从b进入氨气.
故答案为:
(1)①长颈漏斗;②集气瓶.
(2)B; 反应物为固体和液体且不需加热; 2KClO
3
2KCl+3O
2↑.
(3)氧气或者二氧化碳; 2KClO
3
2KCl+3O
2↑或者CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑
(4)D; 将燃着的小木条放在集气瓶口,小木条熄灭证明收集满了.
(5)NH
4Cl+NaOH

NaCl+H
2O+NH
3↑; A; b
分析:(1)熟悉常见仪器,了解名称;
(2)H
2、CO
2、O
2可用上图中的同一种装置来制取,由于这三种气体均可用不加热方式制取,所以可以共用的装置为B;
(3)D装置是向上排空气法,所以该气体应该是密度比空气的大的,所以可以为氧气或者二氧化碳;
(4)收集二氧化碳,由于二氧化碳的密度比空气大,所以应该选用D装置,验满是利用二氧化碳不支持燃烧的性质,所以用燃着的木条放在集气瓶口部观察燃烧情况;
(5)氨气是用氯化铵和消石灰固体加热制得的,所以反应装置应该选用有酒精灯的A.由于氨气密度比空气小,用F装置收集时依然要用向下排空气法,所以是短进长出.
点评:实验发生装置的选择要根据反应物的状态和反应条件,收集装置的选择要根据气体的密度和溶水性.

 2KCl+3O2↑.
2KCl+3O2↑. 2KCl+3O2↑或者CaCO3+2HCl=CaCl2+H2O+CO2↑
2KCl+3O2↑或者CaCO3+2HCl=CaCl2+H2O+CO2↑ NaCl+H2O+NH3↑; A; b
NaCl+H2O+NH3↑; A; b


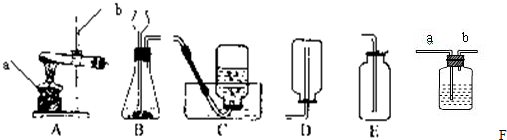

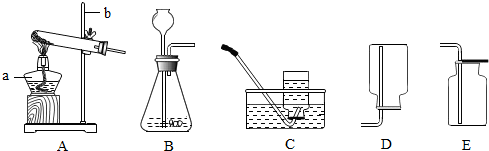
 实验室常用下列装置来制取氧气:
实验室常用下列装置来制取氧气: