
【题目】如图表示稀盐酸和氢氧化钠溶液发生反应过程中溶液的pH的变化,请回答下列问题:
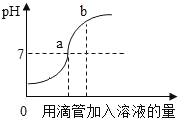
(1)由图可知该实验操作是将_____滴加到另一种溶液中.
(2)所发生中和反应的化学方程式_____.
(3)曲线上b点所含的离子是_____(用符号表示).
(4)下列实际应用中,没有利用中和反应原理的是_____
A 服用含氢氧化铝的药物,可以治疗胃酸过多症
B 用氢氧化钠溶液洗涤石油产品中的残留硫酸
C 用生石灰作干燥剂
【答案】氢氧化钠溶液 NaOH+HCl=NaCl+H2O Na+、Cl﹣、OH﹣ C
【解析】
(1)由图可知起点处pH小于7,随着溶液的加入,溶液的pH由小于7变化为大于7,所以原溶液为稀盐酸,加入的为溶液为氢氧化钠溶液;
(2)反应是盐酸和氢氧化钠反应生成氯化钠和水,对应的化学方程式为![]() ;
;
(3)b点是氢氧化钠过量,所以溶液中有生成的氯化钠和剩余的氢氧化钠,溶液中的离子为![]() 、
、![]() 、
、![]() ;
;
(4)中和反应是酸和碱反应生成盐和水的反应,则有:
A、服用含氢氧化铝的药物,可以治疗胃酸过多症,难溶性碱氢氧化铝和盐酸反应生成氯化铝和水,是中和反应,A选项不正确,不符合题意;
B、用氢氧化钠溶液洗涤石油产品中的残留硫酸,氢氧化钠与硫酸反应生成硫酸钠和水,是中和反应,B选项不正确,不符合题意;
C、用生石灰作干燥剂,是氧化钙和水的反应,生成氢氧化钙,不是中和反应,C选项正确,符合题意。故选C。


科目:初中化学 来源: 题型:
【题目】A~F 为初中化学常见的六种纯净物,且都含有一种相同元素,它们相互间的关系如图所示。已知 A、B、C、D、E 是不同类别的物质,C 俗称纯碱,D 可用于金属除锈,F 是人体中含量最多的物质。(图中“一”表示两端的物质能发生化学反应,“→”表示物质间存在 转化关系,部分反应物或生成物及反应条件已略去)。
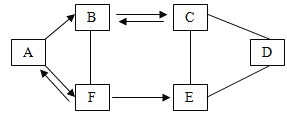
(1)写出 C 的一种用途_____________,写出 D 的化学式___________。
(2)写出 F→E 反应的化学方程式____________, 属于_______________(填基本反应类型)。
(3)将铁屑在 A 中充分燃烧的生成物放入过量的 D 的稀溶液里,(已知:铁元素在氧化亚铁、氧化铁中化合价依次为+2、+3 ,四氧化三铁中铁元素两种化合价都有),所得溶液含有的阳离子为______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海水中有大量化学资源,如氯化镁、氯化钠等,利用海水制备金属镁流程如下:
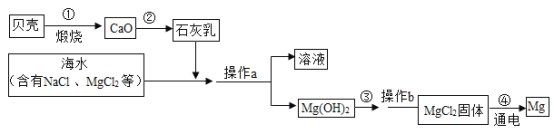
(1)贝壳主要成分的化学式是____。
(2)海水中加入石灰乳发生反应的化学方程式为_____。
(3)实现步骤③的转化,需要加入另一种物质的名称是__;操作b是_。
(4)上述反应未涉及的基本反应类型是_反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一个密闭容器中,有甲、乙、丙、丁、戊五种物质,在一定条件下发生反应,测得反应前后各物质的质量变化量如图所示(图中正数表示物质质量的增加量,负数表示物质质量的减少量,0表示物质质量不变),下列说法正确的是
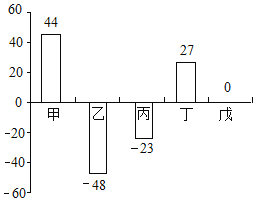
A.甲和丁是该反应中的反应物
B.甲、丁的相对分子质量之比一定为 44:27
C.参加反应的乙、丙的质量比一定为 48:23
D.戊一定是该反应的催化剂
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国科学家侯德榜,在氨碱法的基础上,创立了更为先进的联合制碱法生产纯碱碳 酸钠。某海边工厂利用贝壳、海盐等生产纯碱的主要工艺流程如下:
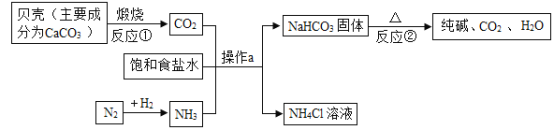
(1)反应①的化学方程式为_____。反应②属于_____反应(填基本反应类型)。
(2)工业上常用_____的方法制取氮气,该过程属于_____变化。
(3)操作 a 的名称是_____,实验室在进行该操作时,用到的玻璃仪器有烧杯、漏斗和_____。
(4)在工农业生产过程中,会排放 CO2 加剧温室效应。下列做法能减少二氧化碳排放的是_____(填序号)。
a 焚烧秸秆肥田 b 提高火力发电量 c 大力使用清洁能源
(5)有一种处理 CO2 的方法,是将 CO2 与氢气在一定条件下反应生成甲烷和水,该反应的化学方程式 为:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一密闭容器中,有甲、乙、丙、丁四种物质,反应前他们的质量如图中白色条形所示,反应后他们的质量如图中黑色条形所示,下列说法正确的是( )
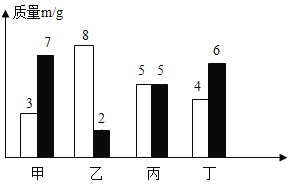
A.该反应中甲是反应物
B.丙一定是该反应的催化剂
C.该反应为化合反应
D.甲和丁的质量变化之比为2:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是地球上最常见的物质之一,下图所示实验中都用到水。下列有关说法错误的是
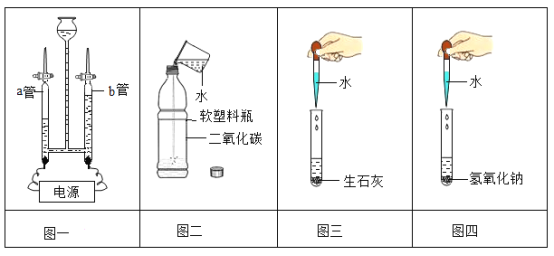
A.图一实验中 b 管内产生的气体有助燃性
B.图二实验加入少量水后,软塑料瓶会变瘪
C.图三实验加入适量水后所得液体可使酚酞溶液变红
D.图四实验中的水参加了化学反应,并放出热量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)下图是硝酸钾和氯化钾固体的溶解度曲线。
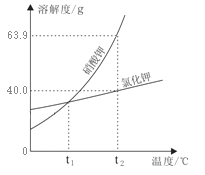
① t1℃时,硝酸钾溶解度______(填“大于”、“等于”或“小于”)氯化钾。
② t2℃时,将等质量的两种固体分别加入100 g水中,充分搅拌后观察到:硝酸钾完全溶解、氯化钾有剩余。则加入的固体质量(m)的取值范围是______________。
③ 将t2℃时的两杯各盛有100 g硝酸钾、氯化钾饱和溶液分别降温到t1℃,下列叙述正确的是___________(填标号)。
A.析出硝酸钾晶体质量小于氯化钾
B.硝酸钾溶液与氯化钾溶液的溶质质量分数相等
C.硝酸钾溶液中溶剂质量大于氯化钾溶液中溶剂质量
(2)某化学小组欲从含有少量氯化钾的硝酸钾样品中,提纯硝酸钾固体。
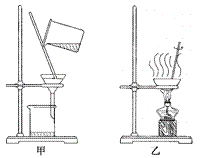
① 可采用的提纯方法是__________(填标号)。
A.冷却热饱和溶液 B.蒸发结晶
② 在提纯过程中,应选择图中_____(填“甲”或“乙”)装置进行分离,该操作中玻璃棒的作用是______________________。
③ 为检验得到的硝酸钾固体是否含有氯化钾,可使用酸化的硝酸银(AgNO3)溶液来检验,该检验方法的原理为_________________(用化学方程式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定锌铜合金中锌的含量,取该合金放入如图 14 盛有稀硫酸的锥形瓶中,发生反应: Zn+H2SO4=ZnSO4+H2↑ 。多次实验后,取平均值所得数据如下表:

反应前 | 充分反应后装置及反应剩余物质质量 | |
装置和足量的稀硫酸质量 | 锌铜合金质量 | |
342.10g | 16.00g | 357.70g |
若不考虑干燥剂吸收空气中的水蒸气,计算:
(1)根据质量守恒定律求生成氢气的质量。
(2)该合金中锌的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com