
| 时 间/s | 0 | 20 | 30 | 40 | 60 | 80 | 100 | 120 |
| 增加的质量/g | 0 | 0.7 | m | 1.2 | 1.5 | 1.6 | 1.7 | 1.7 |
分析 (1)利用数据表中测得的时间与增加的质量关系分析;
(2)利用所绘制的曲线,查出时间为30s时所增加的质量;
(3)根据反应的化学方程式,由生成氨气的质量计算出样品中硝酸铵的质量,利用硝酸铵的质量分数计算即可.
解答 解:(1)根据数据表中测得的时间与增加的质量关系,硝酸铵与氢氧化钠反应所产生的NH3的速率是先快后慢;故填:先快后慢;
(2)根据所绘制的曲线,可估计反应进行至30s时,增加的质量约为1.0g;故选C;
(3)设纯净硝酸铵的质量为x
NH4NO3+NaOH═NaNO3+H2O+NH3↑
80 17
x 1.7g
$\frac{80}{17}=\frac{x}{1.7g}$
x=8g
硝酸铵样品的纯度为:$\frac{8g}{10g}×100%$=80%
答:硝酸铵样品的纯度为80%.
点评 根据质量守恒定律,反应后所得硝酸钠溶液的质量=样品中硝酸铵的质量+溶解所加水的质量+氢氧化钠浓溶液的质量-反应放出氨气的质量.


科目:初中化学 来源: 题型:解答题
| 题号 | 化学方程式 | 评价 | 反应类型 |
| (1) | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | ①B | ②b |
| (2) | 2H2O$\frac{\underline{\;电解\;}}{\;}$H2+O2↑ | ③C | ④a |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| ①将等体积的两种无色液体分别加入A、B两个试管中. ②分别向A、B两试管中同时加入等质量(少量)的二氧化锰,观察现象.  | A试管中无明显现象 B试管中有气泡产生 | A试管中的无色液体是:水(H2O); B试管中的无色液体是:双氧水(H2O2) |
| 猜想 | 验证方法及操作 | 实验现象 | 结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某补钙剂说明书的部分信息如图所示.小明对该补钙剂十分感兴趣,取10片钙片放入100g稀盐酸中,有效成分刚好完全反应(其他成分不与盐酸反应),剩余固体和液体总质量比反应前减少了2.2g,发生反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.请完成下列问题:
某补钙剂说明书的部分信息如图所示.小明对该补钙剂十分感兴趣,取10片钙片放入100g稀盐酸中,有效成分刚好完全反应(其他成分不与盐酸反应),剩余固体和液体总质量比反应前减少了2.2g,发生反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.请完成下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
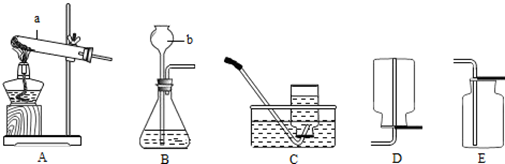
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com