
【题目】有一包粉末,已知其由BaCO3、Cu(NO3)2、Na2SO4、NaCl、NaOH中的几种组成,现对其做以下实验,各步骤均已经充分反应,请回答问题:
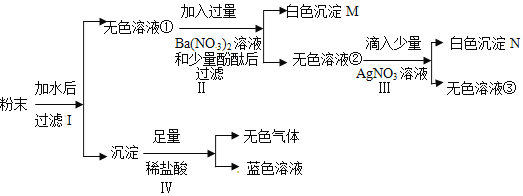
(1)请写出该粉末加水后过滤I得到沉淀的物质化学式:___________________.
(2)步骤Ⅱ所发生反应的化学方程式:_______________________________________________.
(3)无色溶液②中一定存在的溶质(酚酞除外)的化学式:____________________.
【答案】 Cu(OH)2 BaCO3. Na2SO4+Ba(NO3)2=BaSO4↓+2NaNO3. NaNO3 Ba(NO3)2 NaCl.
【解析】(1)加水后的沉淀加入稀盐酸有无色气体和蓝色溶液出现,说明沉淀是氢氧化铜和碳酸钡的混合物,化学式为Cu(OH)2 BaCO3
(2)无色的溶液中加入过量的硝酸钡后,有白色的沉淀生成,说明溶液中一定有硫酸钠,硝酸钡与硫酸钠反应生成硫酸钡沉淀和硝酸钠,反应方程式为Na2SO4+Ba(NO3)2=BaSO4↓+2NaNO3.滴入酚酞后溶液不变为红色,说明无色溶液中没有氢氧化钠;
(3)无色溶液中加入硝酸银,有白色沉淀生成,说明溶液中一定有氯化钠,故无色溶液中有过量的硝酸钡,氯化钠和生成的硝酸钠,化学式为NaNO3 Ba(NO3)2 NaCl.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:初中化学 来源: 题型:
【题目】按下图装置进行实验,倾斜锥形瓶使稀盐酸与固体接触发生反应,瓶内气压的变化如坐标图所示。
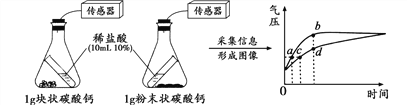
(1)1 g碳酸钙完全反应后,可制得______g 二氧化碳。
(2)对比分析坐标图中的_______点,可知化学反应速率与反应物的接触面积有关。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】家庭养观赏鱼时会在鱼缸里放点“鱼浮灵”,可使水中的含氧量迅速增加。“鱼浮灵”
主要成分是过碳酸钠(xNa2CO3 yH2O2),俗称固体双氧水。某化学兴趣小组对其进行探究。
Ⅰ. “鱼浮灵”的性质研究
实验1:取少量“鱼浮灵”于试管中加水,有持续细小气泡缓慢放出;继续向试管中加有少量MnO2粉末,产生大量气泡。将带火星的木条伸入试管,木条_____________,说明有O2生成,该反应的化学方程式为____________________________。
实验2:取实验1中上层清液,测得溶液pH > 7,说明溶液呈____性(填“酸”、“碱”或“中”);向溶液中滴加足量稀盐酸,产生大量气泡,将产生的气体通入澄清石灰水中,出现浑浊现象,说明有_________生成。
结论:过碳酸钠具有Na2CO3和H2O2的双重化学性质。
Ⅱ. “鱼浮灵”的制备研究
“鱼浮灵”的工业制备流程如下:
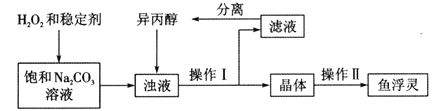
【查阅资料】 异丙醇为有机溶剂,水与异丙醇可以互溶,过碳酸钠在异丙醇中溶解度较小。
稳定剂中MgCl2和 Na2SiO3发生复分解反应,生成一种难溶物将过碳酸钠粒子包裹住,该反应的化学方程式为_________。浊液中加入异丙醇的作用是________。
Ⅲ. “鱼浮灵”的组成研究
利用下图装置进行产品过碳酸钠(xNa2CO3 yH2O2)组成的测定(杂质对测定无影响)。

⑴实验前先缓慢通N2一段时间,加热铜网至红热后,再缓慢滴入过量稀硫酸,直至A中样品完全反应,继续缓慢通N2。继续缓慢通N2的目的是________。
⑵B装置中浓硫酸的作用是_________________________________;
E装置的作用是________________________________________。
⑶若先滴入稀硫酸,后加热铜网,会导致x : y的值__________ (填“偏大”或“偏小”)。
⑷实验测得C装置中铜网增重1.2g,D装置增重2.2g,则x : y =_______。 (写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图一是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线,图二是30℃时,取其中两种固体各1g分别放进盛有10g水的两只试管中,充分振荡后的溶解情况。下列说法正确的是
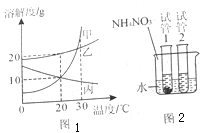
A.甲物质的溶解度比乙物质的溶解度大
B.加入试管1的固体是丙
C.向烧杯中加入硝酸铵固体后,试管2中一定有晶体析出
D.将30℃时甲、乙、丙三种物质的饱和溶液降温到20℃,所得溶液中溶质的质量分数的大小关系是乙>甲=丙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在NaOH和Na2CO3的混合物9.3g中加入一定量的10.0%的稀盐酸,恰好完全反应, 将生成的气体全部通入足量的澄清石灰水中,产生5.0g沉淀。下列说法正确的是( )
A. 题中的一定量是7.3g
B. 反应共产生11.7gNaCl
C. 如用10%的稀盐酸将5.0g沉淀溶解,则所用稀盐酸的量与题中的一定量相等
D. Na2CO3消耗的稀盐酸比NaOH消耗的稀盐酸多
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一包固体粉末可能含有NaNO3、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种,为确定其组成,某同学设计了如下实验方案:
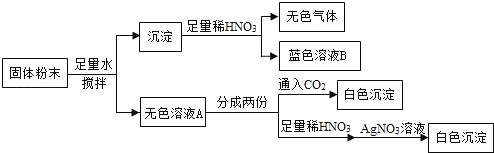
下列判断正确的是( )
A.蓝色溶液B中阳离子只有Cu2+
B.无色溶液A中一定有NaOH
C.原固体粉末一定有NaCl
D.原固体粉末一定有CaCO3、NaOH、NaNO3、CuCl2和Ca(NO3)2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)人类使用的化石燃料主要是煤、石油和________________,直接燃煤会形成严重的酸雨,酸雨是指pH小于______________的降水;
(2)为减少温室气体二氧化碳的排放,可以将二氧化碳进行转化。下图为该反应的微观示意图,根据图示回答下列问题:
反应前 | 反应后 |
| ||
A | B | C | D | |
|
|
|
| |
①以上4种物质中属于有机化合物的是________________(填化学式);
②在反应中C与D质量比为____________________;
(3)氢能是理想的清洁能源。以太阳能为热源,经由铁氧化合物循环分解水的过程如图:
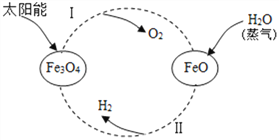
①反应Ⅰ的基本反应类型为___________________;
②写出在一定条件下发生的反应的Ⅱ化学方程式:_____________;
③在上述循环过程中,最终得到的产品是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验设计或结论合理的是![]()
A. 向某固体滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐
B. 除去![]() 溶液中混有的少量
溶液中混有的少量![]() ,可加入适量的
,可加入适量的![]() ,充分搅拌后过滤
,充分搅拌后过滤
C. ![]() 、
、![]() 、
、![]() 、
、![]() 四种离子可在
四种离子可在![]() 的溶液中大量共存
的溶液中大量共存
D. 将带火星的木条伸入到装有气体的集气瓶中,木条不复燃,证明该气体中不含氧气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“低钠盐”可以控制钠的摄入量从而防治高血压等疾病。制备“低钠盐”是在食盐中用NaCl按照配方比例添加食用KCl。国内某些生产厂家为改变“低钠盐”口味还会加入少量镁盐(仅限MgSO4或MgCl2)。
(1)测得某“低钠盐”样品a中只含有NaCl和KCl,该样品中的NaCl和KCl溶于
水时解离出的阴离子都是___________(填离子符号)。
(2)探究某“低钠盐”样品b中是否添加有镁盐,以及添加的是何种镁盐?
【猜想】I、不含镁盐 Ⅱ、含有硫酸镁 Ⅲ、含有氯化镁

【进行实验】
(3)请完成下表(已知BaSO4是难溶于水和酸的白色固体):
假设和现象 | 判断和化学方程式 | |
① | 若现象a为白色沉淀 | 则猜想____不成立。 |
② | 若现象a为_________, 现象b为_________。 | 则猜想Ⅲ成立。写出无色溶液B与硝酸中和反 应的化学方程式_________________。 |
③ | 若现象a、b均 为:产生白色沉淀 | 则猜想____成立。写出无色溶液B与硝酸钡溶液 反应的化学方程式______________。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com