
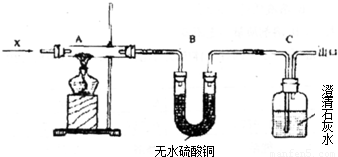
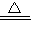 Cu+H2O或C+2CuO
Cu+H2O或C+2CuO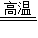 2Cu+CO2↑
2Cu+CO2↑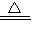 Cu+H2O或C+2CuO
Cu+H2O或C+2CuO 2Cu+CO2↑
2Cu+CO2↑

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:
 实验室有一瓶质量分数较大的盐酸溶液,瓶上标签内容如图所示,请你根据标签上提供的数据与小禹同学一起解答下列问题:
实验室有一瓶质量分数较大的盐酸溶液,瓶上标签内容如图所示,请你根据标签上提供的数据与小禹同学一起解答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 物质 | X | Y | Z | Q |
| 反应前质量(g) | 40.0 | 4.6 | 37.8 | 0.0 |
| 反应后质量(g) | 43.6 | 待测数据 | 4.2 | 8.8 |
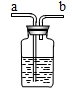
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
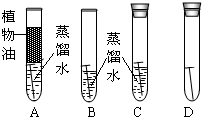
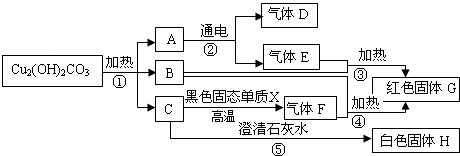
查看答案和解析>>
科目:初中化学 来源: 题型:
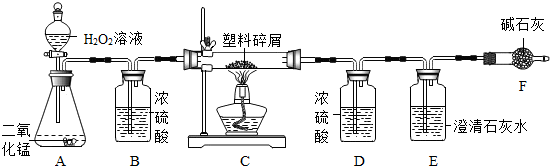
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| ||
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| Ⅰ | 1.2g | ||
| Ⅱ | x | CuO 0.5g | |
| Ⅲ | 1.2g | MnO2 0.5g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com