
【题目】根据下图回答问题。
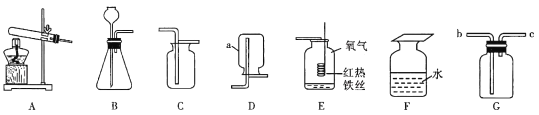
(1)仪器a的名称是_______。
(2)实验室用B装置制氧气的化学方程式为_______。装置E中发生反应的化学方程式为______
(3)实验室常使用仪器G来收集气体,若现在要收集氢气,则气体从__________(填“b”或“c”)端进入;有同学认为只要经过一定的改进措施,氧气也能从该端进入收集,则他的改进措施可能是________。
(4)探究带火星的木条在不同体积分数氧气中的复燃情况,部分实验数据记录如下表所示。已知空气中氧气的体积占1/5。
氧气体积分数/% | 30 | 40 | 60 | 70 |
带火星的木条 | 不变 | 稍亮 | 复燃 | 复燃 |
在集气瓶中注入占其容器50%的水(如图F所示),用排水法收集完氧气后,集气瓶内氧气的体积分数是__________,将带火星的木条伸入该集气瓶中,推测实验现象为______。
【答案】集气瓶 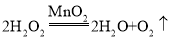
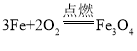 c 在集气瓶中装满水 60% 带火星的木条复燃
c 在集气瓶中装满水 60% 带火星的木条复燃
【解析】
(1)根据所学仪器的名称和用途,a的名称是集气瓶;
故填:集气瓶。
(2)B装置是固体与液体在常温下反应制取气体,用B装置制取氧气,所用的药品是过氧化氢溶液、二氧化锰,反应的化学方程式是: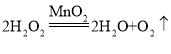 ,装置E中是铁丝在氧气中燃烧生成四氧化三铁,反应的化学方程式是
,装置E中是铁丝在氧气中燃烧生成四氧化三铁,反应的化学方程式是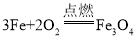 ;
;
故填: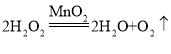
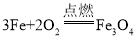
(3)实验室常使用仪器G来收集气体,要收集氢气,氢气的密度比空气的密度小,应从导管口在上的c端进入;氧气从c端进入收集,要采用排水法收集氧气,首先把集气瓶中装满水,氧气从c端进入,利用收集到的气体产生的压强将水排出;
故填:c 在集气瓶中装满水。
(4)设集气瓶的容积是100mL,装满50%的水,收集满氧气后,集气瓶中有50mL的氧气、50mL的空气;50mL的空气中氧气的体积是![]() ,氧气的总体积=50mL+10mL=60mL;则集气瓶中氧气的体积分数=
,氧气的总体积=50mL+10mL=60mL;则集气瓶中氧气的体积分数=![]() ,把带火星的木条伸入该集气瓶中,带火星的木条复燃;
,把带火星的木条伸入该集气瓶中,带火星的木条复燃;
故填:60% 带火星的木条复燃。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】(1)科幻电影《流浪地球》激起人们对太空探索的兴趣,西北工业大学研制的“蓝藻人造叶片系统”让人类移民火星成为可能。在太空极端环境下,蓝藻可以把二氧化碳和水转化为氧气和蔗糖(C12H22O11)。
①C12H22O11属于______(填“无机物”或“有机物”)
②蔗糖分子中氢、氧原子的最简个数比为_______。
③蔗糖中质量分数最大的元素是______。
④电影中当地球和木星靠近时,木星的氢气和地球的氧气混合,为了使地球逃离木星的引力,宇航员引爆了氢气。写出氢气燃烧的化学方程式_______。
(2)华为5G让手机飞起来。制备手机芯片的主要材料是硅,可以用石英砂(主要成分是SiO2)制得。试回答下列问题:
①工业制取硅的主要反应为: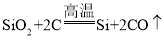 ,生成的一氧化碳中碳元素的化合价为______,该反应的基本反应类型为_____反应。
,生成的一氧化碳中碳元素的化合价为______,该反应的基本反应类型为_____反应。
②二氧化硅是生产玻璃的主要原料之一。下列关于材料的说法错误的是___
A玻璃是无机非金属材料
B玻璃钢属于金属材料
C塑料是有机高分子材料
D生铁和钢都属于合金
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验方案或操作不正确的是( )
A.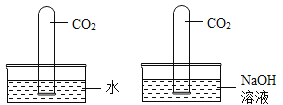 证明CO2与NaOH溶液发生了反应
证明CO2与NaOH溶液发生了反应
B.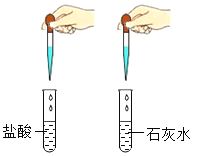 用碳酸钠溶液鉴别盐酸和石灰水
用碳酸钠溶液鉴别盐酸和石灰水
C.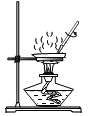 将10%的KNO3溶液变为5%的KNO3溶液
将10%的KNO3溶液变为5%的KNO3溶液
D.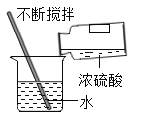 稀释浓硫酸
稀释浓硫酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲和乙在催化剂作用下生成丙和丁,结合微观示意图分析,下列说法正确的是
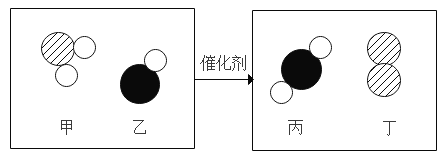

A.上述四种物质都属于化合物
B.生成丙和丁的分子个数比为 4:1
C.该化学反应前后,分子种类保持不变
D.甲中氮、氧元素的质量比为 1:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为探究过氧化氢的分解反应,同学们进行了以下实验。
(查阅资料)过氧化氢分解放热。当氧气低于一定浓度时,可燃物无法燃烧。
(进行实验)
初步探究:探究影响过氧化氢分解速率的因素
序号 | 烧杯1 | 烧杯2 | 烧杯3 | 烧杯4 |
实验操作 |
|
|
|
|
实验现象 | 立即冒大量气泡,烧杯内有 少量白雾出现。 | 5分钟后,有比较大量的气泡冒出。 | 立即冒大量气泡,烧杯内有白雾。 | 立即冒大量气泡,烧杯内有大量白雾。 |
继续探究:重复烧杯1、3、4实验,并分别伸入带火星木条,如下图所示。
实验方案 | 序号 | 实验现象 |
| 烧杯1 | 木条复燃,燃烧很旺 |
烧杯3 | 木条复燃,之后火焰变微弱 | |
烧杯4 | 木条复燃,之后立即熄灭 |
span>
(结论与解释)
(1)写出烧杯1中反应的化学方程式_______。
(2)为证明MnO2和CuSO4能加快过氧化氢的分解速率,应增加的对比实验是_______(填具体操作)。
(3)能证明过氧化氢溶液浓度影响其分解速率的实验是_____(填烧杯的数字序号)。
(4)烧杯内出现大量白雾的原因是_______。
(反思与评价)
(5)烧杯4中木条熄灭的原因可能是_______。
(6)实验室若用双氧水制取氧气来完成木炭燃烧的实验,应选择的试剂是_______(填字母序号)。
A5%过氧化氢溶液 B10%过氧化氢溶液
C20%过氧化氢溶液 D二氧化锰
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中国科学家成功将二氧化碳转化为乙烯(C2H4),反应前后分子种类变化的微观示意图如下。下列说法不正确的是()
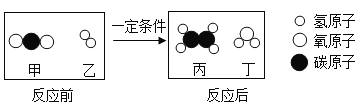
A.甲的相对分子质量为44B.生成物丁为氧化物
C.生成丁18g需要乙2gD.参加反应的甲与乙的分子个数比为1:3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图回答问题。
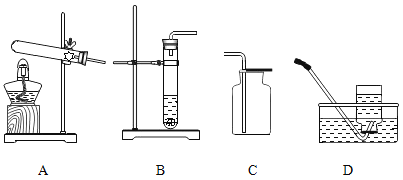
(1)写出实验室制取二氧化碳的化学方程式为__________________。
(2)实验室收集二氧化碳用装置C而最好不用装置D的原因是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】常温下,对100 mL氯化钠饱和溶液进行如图所示实验,下列分析错误的是
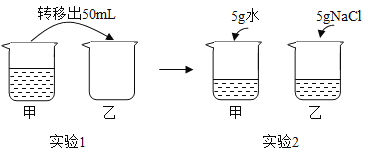
A.实验1后,甲、乙中溶液的溶质质量分数相等
B.实验2后,甲中溶液溶质质量分数减小
C.实验2后, 乙中溶液溶质质量分数增大
D.实验2后,甲、乙中溶液所含溶质质量相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钡是一种可溶性重金属盐。工业上用毒重石(主要成分是BaCO3)制备氯化钡晶体。某实验小组模拟工业上制备氯化钡晶体的流程,设计了实验室中制备氯化钡晶体的方案,实验流程如图所示。(该毒重石样品所含杂质难溶于水,不与酸反应。)
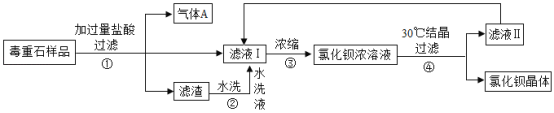
(1)步骤①中发生反应的化学方程式为_____。
(2)滤液Ⅱ是30℃时氯化钡的_____溶液(选填“饱和”或“不饱和”);洗涤氯化钡晶体最适宜的洗涤剂是_____(填字母序号)。
A 30℃水 B 30℃饱和氯化钠溶液 C 30℃饱和氯化钡溶液
(3)关于上述实验方案的相关内容,下列说法不正确的是_____(填字母序号)。
A 氯化钡是一种有毒的物质,使用时应注意安全
B 该实验流程中得到的副产品二氧化碳是重要的化工原料
C 可用重晶石(主要成分是硫酸钡)代替该实验流程中的毒重石,制备氯化钡晶体
D 步骤②将滤渣进行水洗,既能提高氯化钡晶体的产率,又能减少Ba2+对环境的污染
(4)某同学提出,步骤③将滤液Ⅰ浓缩时会产生气体污染物,其化学式为_____。为防止污染,需要对滤液Ⅰ处理后再浓缩。处理滤液Ⅰ用到稍过量甲试剂,该试剂是_____(填字母序号)。
A Ba(OH)2 B BaCl2 C Ba(NO3)2 D BaCO3
(5)实验室有一份混有碳酸钙杂质的碳酸钡样品。分离并提纯碳酸钡的实验步骤如下,请根据要求填空(如图为Ba(OH)2和Ca(OH)2的溶解度曲线):
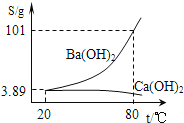
①高温灼烧碳酸钡和碳酸钙的混合物,直至完全分解。碳酸钡和碳酸钙化学性质相似,写出碳酸钡高温分解的化学方程式_____。
②将灼烧后的固体混合物置于80℃的热水中,制成氢氧化钡的热饱和溶液。为减少Ba(OH)2的损失并除去不溶物应进行的操作是_____(选填字母);
A 冷却过滤 B 趁热过滤
③将“②”中滤液冷却结晶并过滤,得到的Ba(OH)2固体中不会含Ca(OH)2,因为_____。
④将“③”中制得的固体溶于水制成溶液。并向制得的溶液中滴加酚酞试剂,再通入二氧化碳。当观察到_____时,Ba(OH)2恰好全部生成BaCO3沉淀,即可停止通二氧化碳。
⑤滤出碳酸钡沉淀,经_____(填一种操作)、干燥后即得到纯净的碳酸钡。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com