
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO2 | CO | 通过足量氢氧化钠溶液,并干燥 |
| B | H2 | 水蒸气 | 通过盛有浓硫酸的洗气瓶 |
| C | N2 | O2 | 通过炽热的木炭 |
| D | NaOH溶液 | Na2CO3 | 加入足量稀盐酸至不再产生气泡 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据二氧化碳会与氢氧化钠反应进行分析;
B、根据浓硫酸有吸水性进行分析;
C、根据碳和氧气反应会生成二氧化碳进行分析;
D、根据氢氧化钠、碳酸钠都会与盐酸反应进行分析.
解答 解:A、二氧化碳会与氢氧化钠反应,混合气通过氢氧化钠溶液,除去了主要物质,故A错误;
B、浓硫酸有吸水性,混合气通过盛有浓硫酸的洗气瓶除去了水蒸气,剩余氢气,故B正确;
C、混合气通过炽热的木炭,生成了二氧化碳,二氧化碳对于氮气也是杂质,故C错误;
D、氢氧化钠、碳酸钠都会与盐酸反应,除去杂质,也除去了主要物质,故D错误.
故选:B.
点评 在解此类题时,首先分析杂质和物质的性质,然后选择适当的试剂只与杂质反应,不与主要物质反应,不会生成新的杂质.


 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 1、测溶液pH | 2、滴加Na2CO3溶液 | 3、滴加AgNO3溶液 |
| 实验操作 | A | B | C |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 现象:有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有HCl | 溶液中有HCl | 溶液中有HCl |
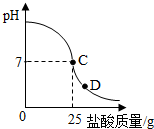 ③所用氢氧化钠溶液中溶质的质量为8g.
③所用氢氧化钠溶液中溶质的质量为8g.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
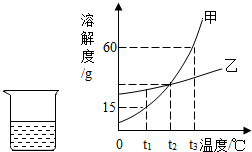 如图是甲、乙两种固体物质的溶解度曲线,烧杯中是t1℃时,将Xg甲物质放入100g水中,充分搅拌后所形成的溶液.下列有关说法正确的是( )
如图是甲、乙两种固体物质的溶解度曲线,烧杯中是t1℃时,将Xg甲物质放入100g水中,充分搅拌后所形成的溶液.下列有关说法正确的是( )| A. | 温度的变化对溶解度影响相对较小的物质是甲 | |
| B. | 在t2℃时,甲、乙溶液的溶质质量分数相等 | |
| C. | X的值一定不大于15g | |
| D. | 将t3℃时,甲、乙饱和溶液降温到t1℃,析出晶体甲比乙多 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
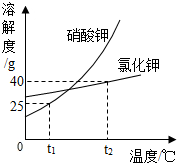 硝酸钾与氯化钾的溶解度曲线如图所示,回答下列问题:
硝酸钾与氯化钾的溶解度曲线如图所示,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com