
 |  |  |  |
| A | B | C | D |
分析 (1)根据实验的方法来分析;
(2))“炔”这类物质的化学式规律是:CnH2n-2,结合质量守恒定律进行分析解答.
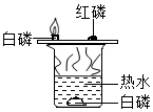
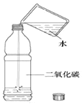
解答 解:(1)A中通过各种金属与酸反应的现象对比分析金属的活动性强弱;B探究了气体能否使澄清的石灰水变浑浊,没有设计对比实验;C中通过铜片上的白磷与红磷的对比,铜片上的白磷与热水中的白磷的对比探究了燃烧的条件;D探究了二氧化碳能否溶于水,没有设计对比实验;故填:C;A与C实验都用了对比的实验方法;
(2)炔烃的书写是有一定规律的,例如:丙炔C3H4,丁炔C4H6,由此可以推知,炔的化学式通式为CnH2n-2,则戊炔的化学式为C5H8;该物质是由碳元素与氢元素组成的,完全燃烧的产物是水和二氧化碳;故填:C5H8;CO2和H2O.
点评 本题考查的是常见的化学实验的探究方法、化学式的书写规律,完成此题,可以依据已有的知识进行.


 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:初中化学 来源: 题型:选择题
 向含有CuCl2和HCl的100g混合溶液中,逐滴加入质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,仅考虑沉淀为Cu(OH)2.则下列说法正确的是( )
向含有CuCl2和HCl的100g混合溶液中,逐滴加入质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,仅考虑沉淀为Cu(OH)2.则下列说法正确的是( )| A. | 整个反应过程中,氯离子个数减少 | |
| B. | P点溶液中的溶质只有一种 | |
| C. | M点溶液比P点溶液中氯化钠的质量分数大 | |
| D. | 沉淀完全时,m1的数值为80 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 序号 | ① | ② | ③ | ④ |
| 物质 | 硫酸铜 | 铁 | 熟石灰 | 纯碱 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 因素 | 第一组 | 第二组 | 第三组 | ||||
| 实验温度 | 20℃ | 20℃ | 20℃ | 20℃ | 20℃ | ||
| 加入溶剂种类 | 水 | 酒精 | 水 | 水 | 水 | ||
| 加入溶剂质量 | 20g | 20g | 10g | 10g | 10g | ||
| 加入固体种类 | 硝酸钾 | 硝酸钾 | 硝酸钾 | 食盐 | 硝酸钾 | ||
| 加入固体质量 | 10g | 10g | 10g | 10g | 10g | ||
| 溶解固体质量 | 6.2g | 0g | 3.1g | 3.6g | 10g | ||
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 夏天,从冰箱里取出的易拉罐过一会儿外壁出现了小水滴--水蒸气凝华 | |
| B. | 二氧化碳可以像到水一样倒入一个容器--二氧化碳的密度比空气大且有流动性 | |
| C. | 夏天雷雨过后,天边会出现一道彩虹--光的直线传播 | |
| D. | 人们将盛液氮的钢瓶漆成黑色--液氮是黑色的 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NO | B. | N2O | C. | N2 | D. | NO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com