
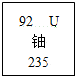
 “七七一矿”是位于大洲镇的一座矿山,盛产核原料铀-235(U-235),根据铀在元素周期表的信息可知( )
“七七一矿”是位于大洲镇的一座矿山,盛产核原料铀-235(U-235),根据铀在元素周期表的信息可知( )| A. | 铀是一种非金属元素 | B. | 铀原子的核外电子数为235 | ||
| C. | 铀原子的中子数为143 | D. | 铀原子的相对原子质量为112克 |
分析 根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符号、元素种类等,进行分析判断即可.
解答 解:A、根据元素周期表中的一格中获取的信息,该元素的名称是铀,属于金属元素,故选项说法错误.
B、根据元素周期表中的一格中获取的信息,该元素的原子序数为92;根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为92,故选项说法错误.
C、根据元素周期表中的一格中获取的信息,该元素的原子序数为92;根据原子序数=核电荷数=质子数,铀原子的质子数为92,相对原子质量为235,由相对原子质量=质子数+中子数,则铀原子的中子数为235-92=143,故选项说法正确.
D、根据元素周期表中的一格中获取的信息,可知元素的相对原子质量为235,相对原子质量单位是“1”,不是“克”,故选项说法错误.
故选C.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法进行分析解题的能力.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:初中化学 来源: 题型:解答题
| 名称 | 赤铁矿 | 菱铁矿 | 磁硫铁矿 |
| 主要成分 | Fe2O3 | FeCO3 | Fe7S8 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验内容 | 实验设计 | |
| A | 除去CO2中少量水蒸气、HCl气体 | 先通过浓硫酸、再通过NaOH溶液 |
| B | 除去NaCl中难溶性杂质 | 溶解、过滤、蒸发 |
| C | 除去KCl溶液中少量的K2CO3 | 加入适量Ca(NO3)2溶液、过滤 |
| D | 鉴别氯化铵、尿素和氯化钾三种化肥 | 取样、加入熟石灰粉末、研磨 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 去除杂质的方法 |
| A | NaCl(Na2CO3) | 加入适量的Ca(OH)2溶液、过滤 |
| B | CaO(CaCO3) | 加水、过滤 |
| C | Fe(Zn) | 加过量FeSO4溶液、过滤 |
| A. | A | B. | B | C. | C |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
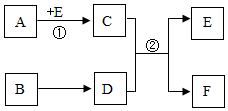 A-F是初中化学常见的物质,它们之间的转化关系如图所示(部分反应物、生成物和反应条件已略去),其中A排放过多会导致温室效应,B是相对分子质量为56的氧化物,C、F都属于盐,且C广泛用于玻璃、造纸、纺织和洗涤剂的生产,D常用于改良酸性土壤,请回答下列问题:
A-F是初中化学常见的物质,它们之间的转化关系如图所示(部分反应物、生成物和反应条件已略去),其中A排放过多会导致温室效应,B是相对分子质量为56的氧化物,C、F都属于盐,且C广泛用于玻璃、造纸、纺织和洗涤剂的生产,D常用于改良酸性土壤,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 某实验小组进行了如图所示的实验.将一定量的红磷点燃后迅速插入集气瓶中并塞住橡皮塞,可以看到红磷燃烧并产生大量白烟.待燃烧停止并冷却到室温后打开止水夹,观察到烧杯中的水进入集气瓶内,进入水的体积大约占原瓶内空气体积的$\frac{1}{5}$.
某实验小组进行了如图所示的实验.将一定量的红磷点燃后迅速插入集气瓶中并塞住橡皮塞,可以看到红磷燃烧并产生大量白烟.待燃烧停止并冷却到室温后打开止水夹,观察到烧杯中的水进入集气瓶内,进入水的体积大约占原瓶内空气体积的$\frac{1}{5}$.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com