
【题目】下图为四种物质的溶解度曲线,下列说法正确的是

A. 0℃时,在100g水中加入40g(NH4)2HPO4,搅拌,完全溶解,再增加1g该物质不能溶解。结论:溶质增加后溶解度降低
B. 30℃时,物质溶解度关系为①>②>③>④
C. 若NH4H2PO4中混有少量NaCl杂质,可在较高温度配成饱和溶液,再降温结晶
D. 要将接近饱和的Ce2(SO4)3溶液变成饱和溶液,操作措施有:加溶质或降温
科目:初中化学 来源: 题型:
【题目】已知A﹣H均为初中化学常见的物质,其中A、C常温下是气体,且组成元素相同,C的固体俗名叫“干冰”,B是赤铁矿的主要成分,E能用于改良酸洗土壤,H是紫红色金属。他们的相互转化关系如图(图中反应条件均已略去):
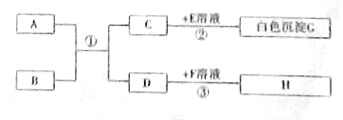
请回答下列问题:
(1)写出E物质的化学式 。
(2)写出反应①的化学方程式 。
(3)反应③的基本反应类型是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我们生活在一个丰富多彩的物质世界中,人类的生产、生活和化学密不可分。
(1)用适当的化学符号填空。
①空气中含量最多的气体_______; ②人体中含量最多的物质是______;
③人体胃液中含有的酸______; ④能做建筑材料的盐是_______。
(2)江阴公共自行车方便了市民出行,也符合“低碳出行”的理念,颇受市民喜爱。
①“低碳出行”中“低碳”指的是较低的______气体排放;
②如图所示自行车中的材料属于金属材料的是________(选填一个序号);

③采用实体轮胎的“共享单车”可有效防止爆胎。而普通自行车夏天易爆胎,请用分子的观点解释“夏天易爆胎”的原因_________;
④扫描二维码可以租用公共自行车,二维码的制作材料一般是用PVC不干胶贴纸。PVC[化学式(C2H3Cl)n]中碳元素和氢元素的质量比为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人们曾用贝壳(主要成分是碳酸钙,杂质不参与反应且不溶于水)和纯碱为原材料制取烧碱,制取流程如下图所示。
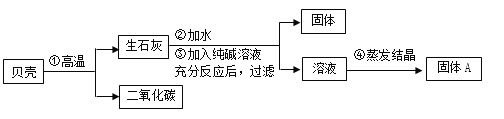
(1)写出步骤①、②的化学方程式①__________;②__________。
(2)固体A的成分可能是纯净的氢氧化钠,还可能是_________、_________(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题:
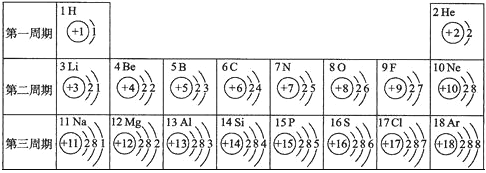
(1)在第三周期中,各原子结构的共同之处是 ;该周期中,各原子核外电子排布的变化规律是 .
(2)在第三周期中,元素类型的变化情况是:从左到右由 元素过渡到 元素,并以 元素结尾.
(3)写出核外电子排布与氖原子相同的阳离子和阴离子符号各一个:
阳离子 ;阴离子 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下图所示装置

(1)写出仪器的名称①______________________,②______________________
(2)用图2制氢气,产生平稳的气流,一段时间后关闭活塞(或弹簧夹),试管中出现的现象是___________________,反应停止。
(3)写出稀释浓硫酸的正确操作_____________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】天气渐暖,春色宜人,某校举行了一场气势宏大的运动会,赛场上同学们沉着应对,稳健发挥,赛出了水平,赛出了友谊。
(1)运动会上的下列用品,主要含有合成有机高分子材料的是________。
A.橡胶跑道 B.纯棉运动服 C.铅球 D.塑料座椅
(2)早晨,学校食堂为同学们准备了以下早餐:炒青菜、鸡蛋、大米粥、馒头,其中蛋白质含量最高的是_____________。
(3)准备比赛用品时,刘翔同学发现铁质的起跑器生锈了,他想用稀盐酸来除铁锈,请写出反应方程式_____________________________________。
(4)比赛中,裁判员高举发令枪,枪声一响,立即产生了大量的白烟,已知枪中火药的主要成分是一种暗红色固体,请画出组成该固体的元素的原子结构示意图_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像能正确反映其对应操作中某物质质量变化关系的是
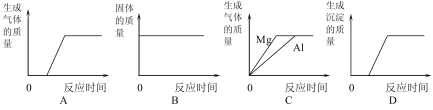
A.将生锈铁钉放入过量的稀盐酸
B.将一定质量的红磷放在盛有氧气的密闭容器中燃烧
C.将等质量的镁和铝分别放入足量的稀硫酸中
D.向氢氧化钠和氯化钡的混合溶液中滴加过量的稀硫酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室用铜辉矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备某种碱式碳酸铜【Cua(OH)b(CO3)cdH2O】的主要实验流程如下图
(1)实验室进行操作I和操作II时,用到的玻璃仪器有:玻璃棒、烧杯和__________。
(2)“浸取”步骤中发生反应(I、II),其中反应I为:2MnO2+Cu2S+□H2SO4=2MnSO4+2CuSO4+S↓+4H2O,在□中的化学计量数是________。
(3)“浸取”步骤中,另一反应II的化学方程式为________________。
(4)滤渣I的成分为MnO2、S和___________。
(5)已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | Mn(OH)2 |
开始沉淀 | 7.5 | 2.7 | 5.2 | 8.3 |
完全沉淀 | 9.7 | 3.2 | 6.4 | 9.8 |
“除铁”步骤中,控制适宜的pH范围为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com