
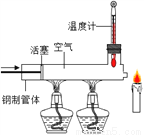
已知蜡烛的着火点约为190℃,蜡烛的火焰由气态蜡燃烧形成。如图所示,在温度计的读数在280℃以上时,快速推动活塞,观察到蜡烛立即熄灭,蜡烛熄灭的主要原因是
A. 隔绝氧气 B. 降低温度到着火点以下
C. 移走可燃物 D. 无法判断
C 【解析】蜡烛的着火点约为190℃,蜡烛的火焰由气态蜡燃烧形成.如图所示,在温度计示数为280℃以上时,快速推动活塞,使气态石蜡被赶走,所以观察到蜡烛立即熄灭,故蜡烛熄灭的主要原因是移走可燃物。A、快速推动活塞,使气态石蜡被赶走,所以观察到蜡烛立即熄灭,故蜡烛熄灭的主要原因是移走可燃物,而不是隔绝氧气,错误;B、快速推动活塞,使气态石蜡被赶走,所以观察到蜡烛立即熄灭,故蜡烛熄灭的主要原因是...科目:初中化学 来源:2018广州市毕业班综合测试化学试卷 题型:填空题
铝合金材料在航空、航天、汽车、机械制造、船舶及化学工业中已大量应用。用铝土矿(含有Al2O3)与NaOH溶液反应可以得到NaAlO2,NaAlO2被CO2酸化生成Al(OH)3,Al(OH)3受热分解生成Al2O3和H2O。
(1)铝合金材料属于___________。(填选项)
A.单质 B.化合物 C.纯净物 D.混合物
(2)Al2O3+2NaOH====2NaAlO2+___________。
(3)HAlO2读作偏铝酸,则NaAlO2读作__________ 。
(4)NaAlO2中铝元素的化合价为___________。
(5)Al(OH)3受热分解的化学方程式为________________________________。
(6)电解熔融的Al2O3可以制得Al和O2,其基本反应类型为_____________________。
D H2O 偏铝酸钠 +3 2Al(OH)3Al2O3+3H2O 分解反应 【解析】(1)合金是在金属中融入了金属或非金属,属于混合物;(2) Al2O3与NaOH溶液反应可以得到NaAlO2和水;(3) HAlO2读作偏铝酸,则NaAlO2读作偏铝酸钠;(4) NaAlO2中钠是+1价,氧是-2价,故铝是+3价;(5) Al(OH)3受热分解生成氧化铝和水,化学方程式为:2Al(OH)3A...查看答案和解析>>
科目:初中化学 来源:安徽省2017-2018学年九年级下学期4月段考化学试卷 题型:单选题
下列肥料属于复合肥料的是
A.NH4NO3 B.KNO3 C.KCl D.Ca(H2PO4)2
B 【解析】 试题分析:复合肥是含有N、P、K三种元素中两种或两种以上的。故选B。查看答案和解析>>
科目:初中化学 来源:福建省2018届初三第二学期期中考试化学试卷 题型:null
铬酸钾 用于金属防锈剂、印染的媒染剂等
用于金属防锈剂、印染的媒染剂等 铬酸钾中铬元素
铬酸钾中铬元素 的化合价为
的化合价为
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:初中化学 来源:江苏省无锡市滨湖区2018届九年级第一次模拟考试化学试卷 题型:单选题
有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按照下列流程进行实验。
下列说法正确的是
A. 滤渣a是CaCO3
B. 白色沉淀b中可能含有MgCO3
C. 滤液中一定存在的溶质是NaCl、BaCl2、NaOH
D. 该白色固体样品中一定含有CaCO3、BaCl2、NaOH、MgCl2,可能含有Na2SO4
C 【解析】A、样品溶于水得到滤渣1.5g,能够全部溶于稀盐酸,且产生0.44g的二氧化碳,说明沉淀一定含有碳酸钙,一定没有硫酸钡; 设产生0.44g的二氧化碳需要碳酸钙的质量为x. CaCO3+2HCl=CaCl2+H2O+CO2↑ 100 44 x...查看答案和解析>>
科目:初中化学 来源:江苏省无锡市滨湖区2018届九年级第一次模拟考试化学试卷 题型:单选题
下图所示实验操作正确的是 ( )

A. A B. B C. C D. D
C 【解析】A、测定溶液pH的方法是:用玻璃棒蘸取少量待测液滴在pH试纸上,然后将pH试纸显示的颜色与标准比色卡进行对照,不能将pH试纸直接浸入待测液中,错误;B、用量筒量取液体的体积,读数时视线要与凹液面的最低处保持水平,错误;C、稀释浓硫酸的方法是将浓硫酸沿着烧杯的内壁慢慢的注入水中并不断的搅拌,不能将水注入浓硫酸中,正确;D、移走蒸发皿要用坩埚钳,错误。故选C。查看答案和解析>>
科目:初中化学 来源:甘肃省2018届九年级第一次模拟考试化学试卷 题型:实验题
下图是化学实验中常用的几种装置。请回答下列问题:



(1)指出有编号的仪器名称:①__________,②________。
(2)写出实验室利用上述A装置制取氧气的化学反应方程式___________________________。
(3)若用F装置干燥生成的氧气,F中盛放的液体试剂是_________,气体应从__________端导入(填“a”或“b”)。
(4)用KClO3制氧气时需加MnO2作催化剂。若在KClO3中加少量的KMnO4,也能加快KCIO3的分解。用文字说明其原因_____________________。
(5)实验室要制取二氧化碳,写出反应的化学方程式___________________________________,
使用G装置制取比B装置的突出优点是___________________,收集CO2的装置是________,(填代号),验满的方法是_________________________________。
酒精灯 长颈漏斗 2KMnO? = K₂MnO? +MnO₂ +O₂↑ 浓硫酸 a 高锰酸钾分解产生了二氧化锰 CaCO3+2HCl==CaCl2+H2O+CO2↑ 控制化学反应的速率 D 燃着的木条放在集气瓶口,熄灭则满 【解析】(1)仪器①是酒精灯,仪器②是长颈漏斗;(2) (2)A装置是用高锰酸钾加热分解生成锰酸钾和二氧化锰和氧气,反应方程式为2KMnO? = K₂MnO? +M...查看答案和解析>>
科目:初中化学 来源:湖北省宜昌市东部2018届九年级下学期期中考试化学试卷 题型:填空题
某废液中可能含有盐酸、氯化钠、硫酸钠、碳酸钠、硝酸钾中的一种或几种。为了检验废液的成分,

小鹏同学的探究过程如下:
⑴原废液中一定含有的溶质是_______________(用化学符号填空,下同);可能含有的溶质是__________。
⑵步骤④发生反应的化学方程式为_________________;
⑶将步骤②的“足量”改为“少量”,不能证明________________的存在;
⑷溶液D中一定含有的阳离子有__________________;反思:检验物质的成分应注意排除干扰因素。
【答案】 Na2SO4、Na2CO3、NaCl KNO3 2HNO3+BaCO3=Ba(NO3)2+H2O+CO2↑ 碳酸钠 钠离子
【解析】(1)加入锌粒无明显现象,说明溶液中没有稀盐酸,加入硝酸钡后后白色沉淀生成,白色的沉淀加入稀硝酸后沉淀部分溶解,说明溶液中一定有碳酸钠和硫酸钠, 溶液B中加入硝酸银有白色沉淀生成,说明B中一定有氯化钠,故原溶液中一定与的物质是Na2SO4、Na2CO3、NaCl;可能含有KNO3;
(2)步骤4 是硝酸与碳酸钡反应生成硝酸钡和二氧化碳和水,反应方程式为2HNO3 + BaCO3 = Ba(NO3)2 + H2O + CO2↑
(3)将步骤②的“足量”改为“少量”,不能证明碳酸钠的存在;溶液中一定存在的是硝酸钠,故阳离子是钠离子;
【题型】流程题
【结束】
28
某班学生分三组分别做了二氧化碳制取和性质验证实验,如下图所示。

甲 乙 丙
实验结束后,老师取两份等质量的丙废液,分别与甲、乙废液混合。将甲废液与丙废液倒入烧杯A中,有白色沉淀生成;将乙废液与丙废液倒入烧杯B中,有气泡产生。
请填空:
(1)甲废液与乙废液所含溶质的成分可能不同的是 (用化学式填空,下同)。
(2)烧杯A中沉淀的成分一定有 。
(3)另取少量丙废液样品,加入足量的氯化钡溶液,有白色沉淀生成。过滤,向滤液中滴加氯化铁溶液,观察到有红褐色沉淀生成,未发现其他明显现象。
由此推测出,丙废液溶质的成分是 ,丙废液与氯化钡溶液反应的化学方程式为 ,烧杯A的上层清液中溶质的成分一定有 。
(1)HCl (2)CaCO3 (3)Na2CO3、NaOH;BaCl2+Na2CO3=BaCO3↓+2NaCl;NaCl、NaOH 【解析】 试题分析:(1)丙中的氢氧化钠与二氧化碳反应生成碳酸钠,碳酸钠与稀盐酸反应生成二氧化碳气体、与氯化钙溶液反应生成碳酸钙白色沉淀,大理石与稀盐酸反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑ ; 甲、乙废液中都有溶质...查看答案和解析>>
科目:初中化学 来源:江苏省泰州市海陵区2018年中考适应性训练化学试卷 题型:单选题
下列有关物质的分类正确的是
A. 纯碱、烧碱属于碱 B. 塑料、生铁属于合成材料
C. 甲烷、碳酸钙属于有机物 D. 水、氧化镁属于氧化物
D 【解析】A、纯碱是碳酸钠,属于盐,错误; B、生铁是合金,不是合成材料,错误; C、碳酸钙是无机物,错误; D、水和氧化镁都是由两种元素组成,其中一种元素是氧元素的化合物,故是氧化物,正确。故选D。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com