
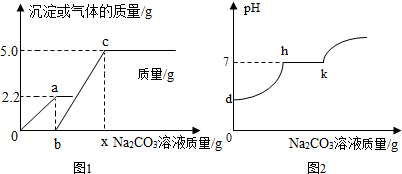
| A�� | ͼ1��0��a�α�ʾ���ɳ����Ĺ��� | |
| B�� | ͼ1��a��ֵΪ106 | |
| C�� | ͼ1��c��ʱ����Һ�е����������� | |
| D�� | ͼ1��b��c�ķ�Ӧ��������Һ��pH�仯�������ͼ2��h��k�����߱�ʾ |
���� ���ݼ����̼�����������ᷴӦ���������������ˣ��ſ�ʼ���Ȼ��Ʒ�Ӧ����ʼ���ɳ����������ߵ�˵���Ѿ���Ӧ���˽��н��
��� �⣺A��ͼ��o��a�α�ʾ���ɵ�������������A����
B��B�����������֪̼�����������ᷴӦ�������Ȼ��Ʒ�Ӧ����ͼʾ��֪̼���������ᷴӦ��������2.2g��̼�������Ȼ��Ʒ�Ӧ�����ɳ���5.0g��������2.2g���������Na2CO3������Ϊy�����ɳ���5.0g����Na2CO3������Ϊz����
Na2CO3+2HCl=2NaCl+CO2��+H2O
106 44
y 2.2g
$\frac{106}{y}$=$\frac{44}{2.2g}$
��ã�y=5.3g��
Na2CO3��Һ������=$\frac{5.3g}{10%}$=53g������ͼ1��a���ֵΪ53����B����
C��c���ʾ̼����ǡ����ȫ��Ӧ����Һ��ֻ����NaClһ�����ʣ���C����
D��ͼ1��b��c�η�Ӧ������̼������Һ���Ȼ��Ʒ�Ӧ��pHֵ���ֲ��䣬����ͼ1��b��c�η�Ӧ��������Һ��pH�仯�������ͼ2��h��k�����߱�ʾ����D��ȷ��
��ѡ��D��
���� �����ؼ�Ҫ֪��ֻ�а����ᷴӦ���ˣ��������Ȼ��Ʒ�Ӧ������������Ϊ���̼�������Ȼ����ȷ�Ӧ������̼��Ƴ�����Ҳ�ᱻʣ��������ܽ���������ῴ��������


 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д� ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
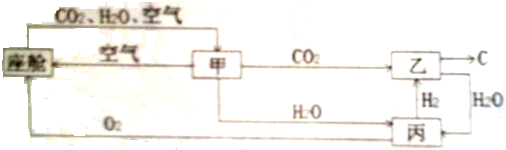
 ��ͼ��5�����ʶ��dz��л�ѧ�������ʣ�ũҵ�ϳ���A��B����ũҩ������Һ��С�ͻ���������A��E�ķ�Ӧ��ȡ�ռC������������Ľ�����ͼ�С�--����ʾ���������������ܷ�Ӧ����ش�
��ͼ��5�����ʶ��dz��л�ѧ�������ʣ�ũҵ�ϳ���A��B����ũҩ������Һ��С�ͻ���������A��E�ķ�Ӧ��ȡ�ռC������������Ľ�����ͼ�С�--����ʾ���������������ܷ�Ӧ����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
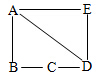
 ��ͼ��Ԫ�����ڱ��й���ҿԪ�ص���Ϣ�����й���ҿԪ�ص�˵������ȷ���ǣ�������
��ͼ��Ԫ�����ڱ��й���ҿԪ�ص���Ϣ�����й���ҿԪ�ص�˵������ȷ���ǣ�������| A�� | ҿԪ�����ڽ���Ԫ�� | B�� | ���ԭ������Ϊ192.2 | ||
| C�� | ԭ�Ӻ�����77������ | D�� | ԭ�Ӻ���������Ϊ77 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ڳ��ڷ����ڿ����е�Ũ����Ũ�Ƚ��� | |
| B�� | ���ڷ���������ƿ�ڵ���ʯ������ | |
| C�� | ������¯����ȵIJ���ֹ��ײ��γ�̿�� | |
| D�� | ����������µĿɽ������ϵĽ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ��һ������CuCl2 | |
| B�� | ��Һ��һ������MgCl2�����ܺ���CuCl2 | |
| C�� | �˳��Ĺ�����һ������Cu��Mg | |
| D�� | �˳��Ĺ�����һ������Fe�����ܺ���Mg |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Һ��������й©ʱ�����̴����̻����� | |
| B�� | �����δ�����IJ˽�ǰ���������ƻ����顱 | |
| C�� | ʹ�ÿɽ������Ͽ��Խ������ɫ��Ⱦ�� | |
| D�� | ������ȱ������ɹ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com