
【题目】如图所示的实验能验证水的组成:
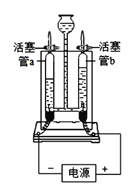
(1)接通直流电源一段时间后,玻璃管b内产生的气体是_________,该管内产生约4g气体时,玻璃管a内产生约_______g气体。
(2)上述实验说明水是由_____________组成的。
(3)该实验中,往电解器玻璃管里加满含有酚酞的硫酸钠溶液(硫酸钠只增强导电性,不发生反应)。在实验过程中,观察到管b电极附近的溶液迅速变红,则该处溶液呈___________(填“酸”“碱”或“中”)性。电解后,待溶液混合均匀后测得溶液的pH=7,说明电解时管a电极附近的溶液呈________(填“酸”“碱”或“中”)性。
(4)该实验中,若水中加入少量硫酸以增强导电性,硫酸不发生反应,则电解后溶液的pH_________(填“增大”“减小”或“不变”)。
【答案】 氧气 0.5 氢元素和氧元素 碱 酸 减小
【解析】本题考查了电解水实验,溶液的酸碱性与pH值的关系。
(1)玻璃管b连接电源的正极,产生的气体体积较小,产生的是氧气;则玻璃管a中产生的是氢气,由化学方程式2H2O ![]() 2H2↑+O2↑可知,生成氢气与氧气的质量比为4:32=1:8,若b管内产生约4g氧气时,玻璃管a内产生约0.5g氢气;
2H2↑+O2↑可知,生成氢气与氧气的质量比为4:32=1:8,若b管内产生约4g氧气时,玻璃管a内产生约0.5g氢气;
(2)电解水生成氢气与氧气,由质量守恒定律可知,水是由氢元素与氧元素组成的;
(3)酚酞遇碱性溶液变红色。在实验过程中,观察到管b电极附近的溶液迅速变红,则该处溶液呈碱性,电解后,待溶液混合均匀后测得溶液的pH=7,说明电解时管a电极附近的溶液呈酸性;
(4)电解水生成氢气和氧,水的质量变小,硫酸质量不变,酸性增强,溶液的pH减小。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:初中化学 来源: 题型:
【题目】下图为 A、B、C 三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( )
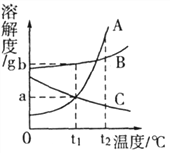
A. t2℃时,三种物质中 B 的溶解度最大
B. t2℃时,取三种物质各 ag 分别放入 l00g 水中,充分溶解,A 和 B 溶液溶质质量分数相同。
C. 将三种物质的饱和溶液分别由 t2℃ 降温到 tl℃, A 溶液中析出的晶体质量最多
D. t1℃将三种物质的饱和溶液分别升温到 t2℃,所得溶液溶质质量分数最大的是 A 溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器)。试根据题目要求,回答下列问题:
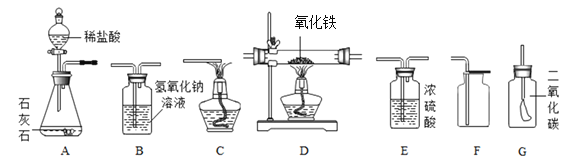
(1)欲在实验室中制备并收集干燥的二氧化碳气体。
①所选仪器的连接顺序为_________________(填写仪器序号字母)。
②仪器A中,发生反应的化学方程式为_____________________。
③若向G装置中倒入适量澄清石灰水,迅速用预先绑有小气球的橡皮塞塞紧,振荡,观察到的气球出现的现象是_______________________。
(2)欲用混有少量二氧化碳的一氧化碳气体还原氧化铁,所选仪器的连接顺序为:混合气体→D→B→C。进行实验时,D装置玻璃管中的现象是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某食盐包装上的部分说明。食盐中加入碘酸钾的目的是补充微量元素___________。

【提出问题】为什么在汤、菜即将煮好时再加入碘盐才能确保碘效?
【查阅资料】碘酸钾的化学式是KIO3,是一种白色粉末,熔点560℃。采用热重分析仪对碘酸钾加热过程展开研究,混合物中碘酸钾的的质量分数(纵坐标)随温度(横坐标)变化的曲线如图10所示。
【猜想假设1】KIO3与KClO3性质类似,受热分解产生O2。
【实验探究1】研究小组进行如图11所示实验,宜选用装置___________进行。验证KIO3分解产生氧气的操作和现象为_________________________。
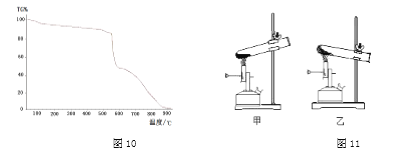
【得出结论1】KIO3受热同时生成碘化钾(KI),反应方程式为_____________________。
【提出新问题】为什么生成KI就会降低碘效?
【查阅资料2】KIO3在人体内转化为I-而被吸收。KI是白色固体,在空气中与O2、CO2、H2O中的两种或三种物质反应生成单质I2而泛黄变质。
【实验探究2】研究小组开展以下实验。
操 作 | 现 象 | 结 论 |
如下图所示,在燃烧匙中放入KI固体,然后分别放置在① ② ③号试管中,数日后观察现象。
| _________ | KI固体在空气中与O2、CO2、H2O共同作用而变质导致碘效降低。 |
【反思提高】
⑴ 讨论后大家认为以上实验方案有所欠缺。甲同学做了补充实验:_____________,数日后观察无明显现象,证明以上结论正确。
⑵ 乙同学推测另一种产物是碳酸盐,请用实验加以证明:______________,证明推测正确。
【拓展应用】生活中鉴别真假加碘盐的方法是:取少量碘盐样品在干净的锅里高温爆炒2分钟,再加入部分未爆炒过的碘盐在碗中混合,加少量白醋,再把刚切好的土豆片浸泡其中,20分钟后若溶液变蓝,则是加碘盐。下列说法不正确的是(_________)
A.实验中土豆片不可用其它食品代替
B.直接将加碘盐放在土豆片上不能呈现蓝色
C.可能是酸性条件下KIO3和KI能反应生成I2
D.烹饪时加醋可能增大食盐中的碘流失
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙、X是初中化学常见的四种物质。下图变化均为初中化学常见反应,其中的每次转化都能一步完成且通过同一基本反应类型实现。下列说法错误的是

A. 若甲是Fe,则丙可以是Zn B. 若甲是CO2,则丙可以是O2
C. 若甲是CO2,则丙可以是Na2CO3 D. 若甲是NaOH,则丙可以是Na2CO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种。同学们为了确定该粉末的成分,进行如下探究:
【提出问题】假设l:红色粉末是铜粉;假设2:红色粉末是氧化铁粉;假设3:红色粉末是铜粉和氧化铁粉。
【设计实验方案】同学们对实验作了如下设想和分析:取5g红色粉末放入硬质玻璃管中,通入一氧化碳片刻后加热至充分反应(实验装置如下图)。
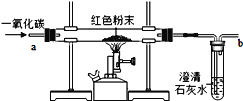
【进行实验】通过实验及分析。若确认假设3成立,则硬质玻璃管中出现的现象是____________。
【反思与评价】(1)实验过程中,硬质玻璃管内发生的化学反应方程式是_________;
(2)实验时通入一氧化碳片刻后再加热的原因是______;
(3)从环保角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是________;
(4)若得到铁的质量为2.24g,则原来混合物中氧化铁粉末的质量分数为_____________。
【知识拓展】实验结束后得到了铜和铁,现为了进一步探究铁和铜的金属活动性强弱,还需要选择的试剂______________(填序号)。
A.碳酸钠溶液 B.稀盐酸 C.氯化锌溶液 D.硝酸铜溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、B、C、D、甲为初中化学常见的物质,甲为参与大气循环的物质,它们之间的转化关系如图所示(反应条件省略)
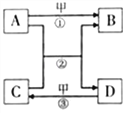
(1)若A、B的组成元素相同,则甲为______(填化学式)
(2)若反应②为复分解反应,则反应②的化学方程式为_________________甲为______(填化学式).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】许多同学都有被蚊子叮过的经历,感觉就是痒。同学们通过化学学习并查阅资料知道:蚊虫叮咬后在人的皮肤内释放出蚁酸刺激皮肤,课外兴趣小组同学决定对蚁酸进行探究。
【提出问题】蚁酸的成分是什么?它有什么性质?
【查阅资料】蚁酸是一种有机酸,化学名称叫做甲酸,化学式为HCOOH;蚁酸在一定条件下会分解生成两种氧化物。
【实验探究一】探究蚁酸的酸性。
(1)向盛有蚁酸溶液的试管中滴加紫色石蕊试液,观察到溶液颜色变成红色,说明蚁酸溶液显酸性;
(2)将锌粒放入盛有蚁酸溶液的试管中,有气泡产生,该气体是________(填名称)。
【实验探究二】探究蚁酸分解的两种产物。
(1)小芳同学根据蚁酸中含有氢氧两种元素,推测出一种生成物是水;
(2)另一种生成物是气体,小敏提出两种猜想:
猜想一:该气体是CO2 猜想二:该气体是________(填化学式);
他们将蚁酸分解产生的气体通过如下装置(铁架台已略去),观察现象。
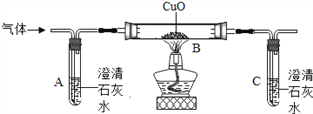
Ⅰ.实验时装置A中无明显变化,则猜想一_________(填“成立”或“不成立”);
Ⅱ.装置B中的现象是________________;从环保角度看,该装置的缺陷是_______________。
【拓展】当你被蚊虫叮咬后,在叮咬处涂抹一些物质可减轻痛痒。下列物质中,你不会选择的物质是___________。
A.风油精 B.苏打水 C.肥皂水 D.食醋
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类的生存和发展离不开能源和资源。
(1)家用燃料的更新过程如下:煤→液化石油气或管道煤气→天然气。
①下列有关家用燃料更新的理由,正确的是___________。
A.天然气属于可再生能源 B.气体燃料比固体燃料利用率更高
C.天然气作为燃料可避免温室效应的发生 D.煤仅用作燃料烧掉浪费资源
②天然气的主要成分是甲烷,在空气中完全燃烧的化学方程式为__________。
(2)人类每年都要从大自然中提取大量的金属,用于满足生产和生活的需要。
①高炉炼铁过程中,焦炭的作用是提供热量和___________。
②生活中将生铁制成铁锅,是利用其__________和延展性,将铁丝放在潮湿的空气中(如图所示),一段时间后,观察到铁丝生锈,原因是铁与_____和_____(均填化学式)同时接触,同时观察到导管内液面上升;打开K,滴加稀盐酸,观察到导管内液面下降且导管口有气泡冒出,用化学方程式解释______。
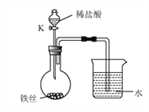
③稀盐酸可以除去铁器表面的铁锈,写出该反应的化学方程式________。实验中若需配制74g质量分数为10%的稀盐酸,需要质量分数为37%的浓盐酸(密度为1.18g/cm3)________ g,加水________mL。若用量筒量取浓盐酸时俯视读数,所配溶液中溶质的质量分数________10%(填“大于”、“小于”或“等于”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com