
【题目】水是生命源泉,我们应该爱护水资源,节约用水。下列说法正确的是
A.学校厕所水龙头的上方适合张贴的标志是![]()
B.过滤能除去天然水中的所有杂质
C.活性炭的吸附作用可使海水转化成淡水
D.河水经过吸附、静置、过滤、消毒、蒸馏等处理得到纯净的水
 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:初中化学 来源: 题型:
【题目】人类的生产生活离不开金属。
(1)在地壳里含量最多的金属元素是 ____________(填元素符号) 。
(2)下列铜制品的用途中,利用金属导电性的是 ____________(填字母)。
A 铜火锅 B 铜导线 C 铜 钟 D 铜 钱
(3)下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝。金属大规模被使用的先后顺序跟_______(填字母)关系最大。
A 地壳中金属元素的含量 B 金属的导电性 C 金属的活动性
(4)现有一包由 5.6 g 铁、7.2 g 镁、1.0 g 碳混合而成的粉末,把它加入一定量的氯化铜溶液中。写出铁和氯化铜溶液反应的化学方程式 ____________,实验结束后,测得剩余固体中含有三种物质。则剩余固体的质量不可能是 ____________(填字母)。
A 26.2 g B 26.6 g C 26.0 g D 25.8 g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(一)工业上炼铁炼钢和轧制钢材的主要流程如图,已知生铁的含碳量为2%~4.3%钢的含碳量0.03%~2%。
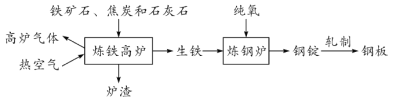
(1)炼铁的固体原料需经过粉碎,其目的是________________。
(2)炼钢炉中,通入纯氧的目的是 ______。将钢锭轧成钢板,体现了金属的__________性。
(3)钢铁制品可能会生锈,写出用稀硫酸除锈反应的化学方程式______________。
(二)下图中是初中化学六种常见物质之间的转化关系图。已知A、D、F均为单质,其中D、F为金属单质,D的合金是使用最多的金属材料;B为氧化物,C是一种常见的酸,E(相对分子质量为160)的溶液呈蓝色。试回答下列问题:(框图中的反应条件和某些生成物已略去)。
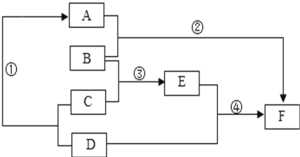
(1)请写出下列物质的化学式:B_____________,D_____________,F_____________。
(2)上述反应中,不属于置换反应的是_____________(填序号)。
(3)请写出反应④的化学方程式:_________________
(4)请写出E在生产生活中的一种用途__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某盐酸中混有少量的 MgCl2,小明为了测定该盐酸混合液中 HCl 的质量分数,进行如下图实验:
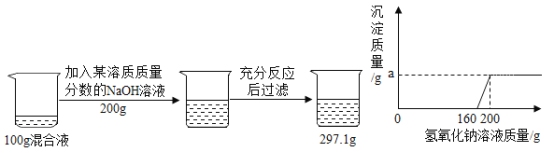
请结合如图实验数据,完成以下计算:
(1)观察上图的实验过程确定坐标图中 a 的数值为_____;
(2)所加NaOH 溶液的溶质质量分数为 20%,求该盐酸混合液中HCl 的质量分数。_____(写出计算过程;化学方程式:NaOH+HCl=NaCl+H2O;2NaOH+MgCl2=2NaCl+Mg(OH)2↓)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常利用以下装置完成气体制备及性质实验,请回答:
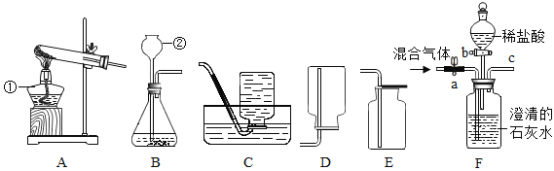
(1)指出编号仪器的名称:①______________,②________________。
(2)以上A装置有一处明显的错误,请加以改正______________,利用改正后的装置继续完成后面的实验。
(3)欲使用高锰酸钾制取氧气,应选择的A装置,反应方程式为_______;为防止高锰酸钾粉末进入导管,应采取的措施是________。
(4)工业上常需分离CO、CO2的混合气体,某同学采用装置F也能达到分离该混合气体的目的,操作步骤如下:
①关闭活塞b,打开活塞a,通入混合气体,可从导管c处收集到_____气体。
②然后,关闭活塞a,打开活塞b,又可收集到另一种气体,写出F中发生反应的化学方程式______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶解是生活中的常见现象。
(1)A、B、C三种物质的溶解度曲线如图所示。
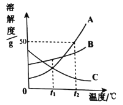
①t1℃时,______两种物质的饱和溶液中溶质质量分数相等。
②t2℃时,把60gA放入100g水中,充分搅拌得到A的溶液溶质和溶液的质量比为_____(填最简比)。
③将t2℃的A、B、C三种物质的饱和溶液都降温至t1℃,所得三种溶液的溶质质量分数由大到小关系是_______。
(2)下表是氯化钠和硝酸钾两种物质在不同温度时的溶解度,根据表中信息回答问题。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
硝酸钾 | 13.3 | 31.6 | 63.9 | 11. | 169 | 246 | |
①40℃时,硝酸钾的溶解度________氯化钠的溶解度(填“>”“=”或“<”)。
②取100mL水,加入30g氯化钠,充分搅拌,恢复至20°C,得溶液A,A溶液属于_______溶液(填“饱和”或“不饱和”);加热A溶液至60°C,再加10g氯化钠,搅拌,得溶液B。B溶液质量是_______g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】X、Y、Z三种物质的溶解度曲线如图所示,下列说法正确的是( )
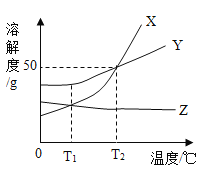
A.Y的溶解度为50 g
B.T2℃时,X、Y两种物质的溶解度相等
C.T1℃时,三种物质的溶解度由大到小的顺序是Y>X>Z
D.T2℃时,50 g H2O与50 g X混合,可得到100 g X的饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法正确的是
A.镁和金属X的混合物共2.4g加入足量的稀硫酸,充分反应后得到0.22g氢气,则金属X可能是Zn
B.t°C某饱和的氢氧化钙溶液加入少量的生石灰,充分反应后,恢复到t℃,则溶液的溶质质量分数不变
C.农业科研实验室用一定量的NH4NO3和KH2PO4的固体混合物配制无土栽培营养液,已知固体混合物中氮元素的质量分数为28%,则固体混合物中KH2PO4的质量分数为20%
D.某样品含有氢氧化钾、碳酸钾和水三种物质。室温下,向该样品中加入浓度为14.6%的稀盐酸100g,恰好完全反应得到中性溶液,蒸干该溶液得到固体质量为7.45g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)铁是生产、生活中使用最广泛的一种金属。
①现在的中国高铁与轨道交通已经成为了中国一张全新的名 片,中国的高铁出口也正在引领着世界铁路变革。钢轨属于_____(填“单质”“合金”“氧化物”之一)。

②碳化铁(Fe3C)在冶金上称为渗碳体,可由铁粉渗碳来制得。它有优良的切削加工性能,广泛用于机械制造。碳化铁在足量的空气中高温煅烧,生成四氧化三铁和能使澄清石灰水变浑浊的气体,该反应的化学方程式为_____。
(2)我国著名化学家侯德榜创立的侯氏制碱法,是以海水“晒盐”得到的氯化钠为原料, 同时制得 Na2CO3 和 NH4Cl 产品。Na2CO3 和 NH4Cl 的溶解度曲线如图所示。
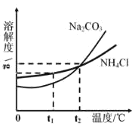
试回答下列问题:
①t2℃时,Na2CO3溶液的溶质质量分数_____NH4Cl 溶液的溶质质量分数(填“大于”“等于”“小于”“无法判断” 之一)。
②将t2℃时等质量的Na2CO3 和NH4Cl 的饱和溶液均降温至t1℃时,Na2CO3 溶液的溶质质量分数_____NH4Cl 溶液的溶质质量分数(填“大于”“等于”“小于”“无法判断”之一)。
③若Na2CO3 固体中含少量NH4Cl,提纯Na2CO3 可采用_(填“蒸发结晶” 或“降温结晶”之一)的方法。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com