
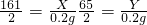
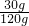 ×100%=25%;
×100%=25%; =
= (或者
(或者 =
=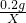 )
)

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:初中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:初中化学 来源:2012-2013学年北京市东城区中考一模化学试卷(解析版) 题型:填空题
金属是人类生活中的常用的材料.
(1)下列生活用品中,主要利用金属导热性的是 (填字母序号).

(2)工业上用赤铁矿(主要成分是氧化铁)冶炼铁的化学方程式是 .
(3)现有锌片、铜片、稀硫酸、硫酸锌溶液和硫酸铜溶液5种物质,某同学欲探究锌和铜的金属活动性顺序,选择的一组试剂是 ,其现象是 .
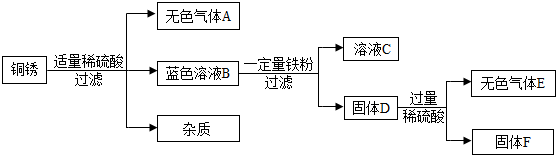
(4)该同学查阅资料得知,铜锈的主要成分是碱式碳酸铜【Cu2(OH)2CO3】,他以铜锈为原料设计并完成如下实验(杂质不与稀硫酸反应,且不含铜元素.图中部分物质略去).

①溶液C中所含的溶质是 .
②已知铜锈中Cu2(OH)2CO3的质量分数是10%,固体F的质量是1.28g,则铜锈中含Cu的质量分数是
(结果精确至0.1%).
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源:2013年北京市东城区中考化学一模试卷(解析版) 题型:填空题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com