
| 序号 | 样品 | 量筒起始 读数/mL | 量筒最终 读数/mL | 所需时间/min |
| 1 | 1.0g铁粉、0.2g碳和10滴水 | 100 | 72 | 约120 |
| 2 | l.0g铁粉、0.2g碳、10滴水和少量NaCl | 100 | 72 | 约70 |
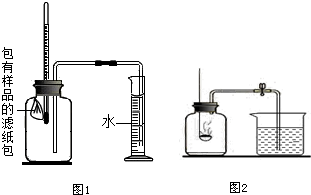
分析 (1)对实验①和②的数据进行比较,即可得出NaCl可以加快铁锈蚀的速率;
(2)根据信息“实验开始后,广口瓶内温度有所上升”进行分析;
(3)通过空气体积的变化得出,空气中氧气的体积分数.造成测得氧气的体积分数小于五分之一的因素可以从以下方面考虑:装置是否漏气;药品的用量是否充足;装置是否冷却到室温等,据此分析.
解答 解:(1)实验①和②之间唯一的变量为是NaCl,根据含有NaCl的实验②,反应所需的时间较短,得到NaCl能加快铁锈蚀的速率;
(2)根据信息“实验开始后,广口瓶内温度有所上升”,可以直接得出铁锈蚀的过程是放热的过程;
(3)因为量筒内液体减少的体积即为广口瓶内所含有的全部氧气的体积,所以氧气的体积含量是$\frac{(100-72)mL}{134mL}$×100%=20.9%.
A、实验前没有将弹簧夹夹紧,瓶内的气体处于热膨胀状态有一部分逸出,使进入集气瓶中的水的量偏大,故A不可能;
B、实验装置漏气,由于冷却至室温时瓶外空气进入瓶中,会导致进入水的量偏小,故B可能;
C、实验中所取红磷过量时,红磷能够将集气瓶中氧气全部反应掉,因此测得氧气的体积分数约为五分之一,故C不可能;
D、实验中所取红磷的量不足时,会导致装置内氧气不能全部消耗,因此使测得氧气的体积分数会小于五分之一,故D可能.
故选BD.
故答案为:(1)氯化钠会加速(或影响)铁的锈蚀速度
(2)放热;(3)20.9;BD
点评 本题考查学生根据铁生锈的条件和防止金属的腐蚀的方法以及探究测定空气中氧气含量的误差分析,并将知识应用到生活中去.


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ②③④ | C. | ②③ | D. | ①②③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
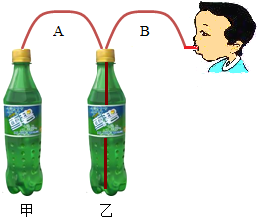 如图所示,小柯制作了一个家庭制氧装置供人呼吸.该制氧装置由2个饮料瓶、2根软管和药剂构成,药剂包括过氧碳酸钠(2Na2CO3•3H2O2)和二氧化锰.制氧时,先在两个饮料瓶中加入适量的水,再往甲瓶中加入药剂,产生的气体通过A、B管从乙瓶导出,供人吸氧.
如图所示,小柯制作了一个家庭制氧装置供人呼吸.该制氧装置由2个饮料瓶、2根软管和药剂构成,药剂包括过氧碳酸钠(2Na2CO3•3H2O2)和二氧化锰.制氧时,先在两个饮料瓶中加入适量的水,再往甲瓶中加入药剂,产生的气体通过A、B管从乙瓶导出,供人吸氧.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 化学反应事实 | 影响化学反应的因素 |
| A | 铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧 | 反应物浓度 |
| B | 碳在常温下不与氧气发生反应,而在点燃时能与氧气反应 | 反应条件 |
| C | 双氧水在常温下较难分解,而在加入二氧化锰后迅速分解 | 催化剂 |
| D | 铜片在空气中很难燃烧,铜粉在空气中较易燃烧 | 反应物的种类 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 用小苏打治疗胃酸过多 NaHCO3+HCl=NaCl+H2O+CO2↑ | |
| B. | 实验室用过氧化氢溶液制取氧气 2H2O2=2H2O+O2↑ | |
| C. | 用盐酸除去铁锈 Fe2O3+6HCl=2FeCl3+3H2O | |
| D. | 用石灰水检验二氧化碳 Ca(OH)2+CO2=CaCO3+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | B. | 2NaNO3+CuCl2=2NaCl+Cu(NO3)2 | ||
| C. | Fe(OH)3+3HCl=FeCl3+3H2O | D. | CuCO3+2NaOH→Cu(OH)2↓+Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ${\;}_{3}^{4}$He | B. | ${\;}_{2}^{3}$He | C. | ${\;}_{2}^{4}$He | D. | ${\;}_{3}^{3}$He |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com