
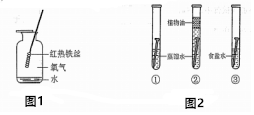
 铁是生活中的常见金属,请回答下列问题:
铁是生活中的常见金属,请回答下列问题:分析 (1)根据铁丝在氧气中燃烧的注意事项来分析;
(2)根据铁生锈的条件是跟空气和水同时接触分析.
解答 解:(1)铁丝在氧气中燃烧实验,集气瓶底部要预先放少量的水或铺一层细沙,目的是防止生成物熔化溅落下来炸裂集气瓶;故填:防止生成物熔化溅落下来炸裂集气瓶;
(2)①中的铁钉既与水接触,又与氧气接触,所以铁钉发生了锈蚀,而②中的铁钉只与水接触没有锈蚀,说明铁钉锈蚀需要氧气;实验③中的铁钉锈蚀速率比①中的快,这说明该实验在探究食盐能否加快铁的锈蚀速率;故填:氧气;①;食盐能否加快铁的锈蚀速率.
点评 本题主要考查学生对铁生锈的条件这一知识点的掌握情况,尤其强调铁同时直接和氧气、水接触这一点.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
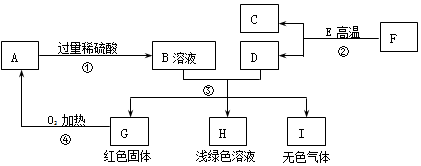
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2KClO3$\frac{\underline{\;△\;}}{\;}$2KCl+3O2↑ | B. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | ||
| C. | 2Ag+Cu(NO3)2═2AgNO3+Cu↓ | D. | 2HCl+Na2SO4═2NaCl+H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
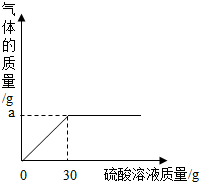 草木灰属于农家肥料,它的主要成分是碳酸钾,还有硫酸钾,氯化钾等,为测定某草木灰样品中的有效成分,取100g该草木灰于烧杯中,不断滴入稀硫酸溶液,当滴入30g稀硫酸时,不再有气泡产生,此时烧杯中的残余混合物质量为127.8g,碳酸钾与硫酸反应的化学方程式为K2CO3+H2SO4=K2CO4+CO2↑+H2O
草木灰属于农家肥料,它的主要成分是碳酸钾,还有硫酸钾,氯化钾等,为测定某草木灰样品中的有效成分,取100g该草木灰于烧杯中,不断滴入稀硫酸溶液,当滴入30g稀硫酸时,不再有气泡产生,此时烧杯中的残余混合物质量为127.8g,碳酸钾与硫酸反应的化学方程式为K2CO3+H2SO4=K2CO4+CO2↑+H2O查看答案和解析>>
科目:初中化学 来源: 题型:填空题
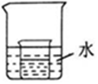
 我们已经知道空气的主要成分是氮气和氧气,如图所示为测定空气中氧气含量的实验装置示意图,图中玻璃管里的活塞可以左右移动,活塞的左端管内有密封的空气,活塞右端的玻璃管口跟空气相通,实验开始前活塞处在刻度5处.请回答下列问题:
我们已经知道空气的主要成分是氮气和氧气,如图所示为测定空气中氧气含量的实验装置示意图,图中玻璃管里的活塞可以左右移动,活塞的左端管内有密封的空气,活塞右端的玻璃管口跟空气相通,实验开始前活塞处在刻度5处.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 下表提供了硝酸钾固体在不同温度时的溶解度.
下表提供了硝酸钾固体在不同温度时的溶解度.| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com