
| 反应前 | 反应后 | |
| 过氧化氢溶液质量/g | 二氧化锰质量/g | 固体与液体混合物质量/g |
| 68.0 | 0.1 | 66.5 |
分析 (1)根据质量守恒定律计算生成氧气的质量;
(2)根据过氧化氢在二氧化锰的催化作用下生成水和氧气,结合氧气的质量,计算出参加反应的过氧化氢的质量,再计算质量分数.
解答 解:(1)根据质量守恒定律可知,生成氧气的质量为:68g+0.1g-66.5g=1.6 g;
(2)解:设参加反应的H2O2的质量为x,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 1.6 g
$\frac{68}{x}=\frac{32}{1.6g}$
x=3.4 g
所用的过氧化氢溶液中H2O2的质量分数:$\frac{3.4g}{68g}$×100%=5%
故答案为:
(1)1.6g;
(2)该同学所用过氧化氢溶液的溶质质量分数是5%.
点评 本题主要考查了化学方程式的计算,难度不大,需要认真分析反应应用的原理,然后结合题中所给的数据进行计算.


科目:初中化学 来源: 题型:解答题
 某同学家的下水管道堵塞了,于是他买了一瓶“管道疏通剂”(部分说明如图).疏通剂是利用铝与氢氧化钠溶液反应产生气体且放出大量的热,以加快氢氧化钠与毛发等淤积物的作用,反应原理为:
某同学家的下水管道堵塞了,于是他买了一瓶“管道疏通剂”(部分说明如图).疏通剂是利用铝与氢氧化钠溶液反应产生气体且放出大量的热,以加快氢氧化钠与毛发等淤积物的作用,反应原理为:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 甲、乙、丙是三个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题:
甲、乙、丙是三个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题:| 物质 | 镁 | 含0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧现象 | 剧烈燃烧,发出耀眼白光,无火星 | 剧烈燃烧,极少火星 | 剧烈燃烧,少量火星 | 剧烈燃烧,火星四射 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
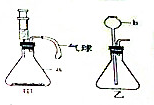 如图所示两套装置,请回答:
如图所示两套装置,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
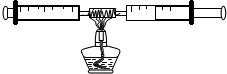 如图所示是某同学测定空气中氧气含量的装置.玻璃管中装的是细铜丝.
如图所示是某同学测定空气中氧气含量的装置.玻璃管中装的是细铜丝.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com