在7.36gCaCO3和MgCO3组成的混合物中加入足量的盐酸,产生的CO2全部被48g质量分数为10%的NaOH溶液吸收,恰好完全反应.把吸收后溶液在减压低温的条件下蒸干,可得7.6g固体.试求吸收的CO2是多少克?(提示:CO2在足量的情况下,与NaOH溶液反应生成NaHCO3).
【答案】
分析:首先由氢氧化钠溶液的质量和质量分数通过氢氧化钠分别全部转化为碳酸钠和碳酸氢钠的化学方程式分别计算出生成碳酸钠和碳酸氢钠的质量,再结合得到固体的质量确定所得固体的组成.
由固体的质量和氢氧化钠的质量通过上述两个反应的化学方程式可以计算出生成碳酸钠的质量和碳酸氢钠的质量.
由碳酸钠和碳酸氢钠的质量可以计算出分别生成碳酸钠和碳酸氢钠的二氧化碳的质量,进而计算出吸收二氧化碳的质量.
解答:解:氢氧化钠的质量为48g×10%=4.8g
设氢氧化钠全部转化成碳酸钠时所得碳酸钠的质量为x.
2NaOH+CO
2=Na
2CO
3+H
2O
80 106
4.8g x

=

,x=6.36g<7.6g
设氢氧化钠全部转化成碳酸氢钠时所得碳酸氢钠的质量为y.
NaOH+CO
2=NaHCO
340 84
4.8g y
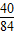
=
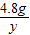
,y=10.08g>7.6g
说明7.6g固体中既有碳酸钠,又有碳酸氢钠.
设能反应生成碳酸钠的氢氧化钠的质量为z,生成碳酸钠的质量为w.
2NaOH+CO
2=Na
2CO
3+H
2O
80 106
z w

=
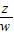
NaOH+CO
2=NaHCO
340 84
4.8g-z 7.6g-w

=

解上面两个等式得w=4.24g
设反应生成碳酸钠的二氧化碳的质量为m.
2NaOH+CO
2=Na
2CO
3+H
2O
44 106
m 4.24g
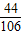
=
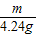
,m=1.76g
设反应生成碳酸氢钠的二氧化碳的质量为n.
NaOH+CO
2=NaHCO
3 44 84
n 7.6g-4.24g=3.36g

=

,n=1.76g
吸收二氧化碳的质量为1.76g+1.76g=3.52g
答:吸收二氧化碳的质量为3.52g.
点评:本题主要考查有关化学方程式的计算,难度较大.通过本题可知:反应物的量不同,生成物也可能不同.解答本题的关键是先判断出生成物是否相同,其次是利用数据间的关系计算出要求的量.

 =
= ,x=6.36g<7.6g
,x=6.36g<7.6g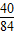 =
=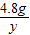 ,y=10.08g>7.6g
,y=10.08g>7.6g =
=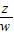
 =
=
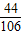 =
=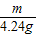 ,m=1.76g
,m=1.76g =
= ,n=1.76g
,n=1.76g