
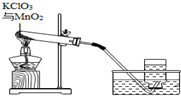
 ij��ȤС������ͼ��ʾװ����ȡ�������Թ��й����������ʱ��仯�������������ȡ������ʣ�����������ˮ����ܽ���ˣ����ն������̹��壬���õ��Ȼ�����Һ100g ��O��16 Cl��35.5 K��39��
ij��ȤС������ͼ��ʾװ����ȡ�������Թ��й����������ʱ��仯�������������ȡ������ʣ�����������ˮ����ܽ���ˣ����ն������̹��壬���õ��Ȼ�����Һ100g ��O��16 Cl��35.5 K��39��| ����ʱ��/min | 0 | t1 | t2 | t3 | t4 |
| ��������/g | 28.0 | 23.2 | 18.4 | a | 18.4 |
���� ��1�����ݱ��е����ݹ���������t2��t4ʱ����18.4g������aΪ18.4���з�����
��2�����������غ㶨�ɼ�������������������
��3�����ݻ�ѧ����ʽ���������������м��㣮
��� �⣺��1���ɱ��е����ݹ���������t2��t4ʱ����18.4g������t3ʱ����������Ѿ������ˣ�aΪ18.4��
��2�����ɵ���������Ϊ��28g-18.4g=9.6g��
��3���跴Ӧ�����Ȼ��ص�����Ϊx��
2KClO3$\frac{\underline{MnO_2}}{��}$2KCl+3O2����
149 96
x 9.6g
$\frac{149}{x}$=$\frac{96}{9.6g}$
x=14.9g
�Ȼ�����Һ�����ʵ���������Ϊ��$\frac{14.9g}{100g}$��100%=14.9%��
�ʴ�Ϊ����1��18.4��
��2��9.6��
��3��14.9%��
���� ������Ҫ����ѧ�����ü��跨�ͻ�ѧ����ʽ���м�����ƶϵ�����������ʱҪע��淶�Ժ�ȷ�ԣ�


 ����νӽ̲���ĩ���Ԥϰ�人������ϵ�д�
����νӽ̲���ĩ���Ԥϰ�人������ϵ�д� ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
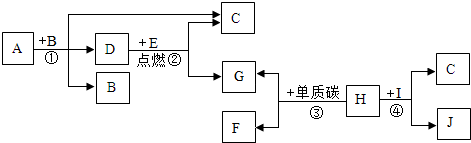
 ������ѧ�Ļ�ѧ֪ʶ������������
������ѧ�Ļ�ѧ֪ʶ�������������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
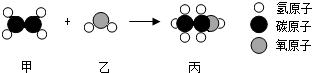
| A�� | �÷�Ӧ���ڻ��Ϸ�Ӧ | |
| B�� | �÷�Ӧ�з��Ӻ�ԭ�ӵ���������˸ı� | |
| C�� | ����̼������Ԫ�ص�������Ϊ6��1 | |
| D�� | �ס����ֱ�����������ȫȼ�գ�������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com