
| A. | 上浮 | B. | 悬浮 | C. | 下沉 | D. | 无法确定 |
科目:初中化学 来源: 题型:填空题
| 气体 性质 | H2 | CO2 | O2 | N2 | Cl2 |
| 气体的沸点/℃ | -252 | -78 | -183 | -196 | -34 |
| 被吸附体积/mL | 4.5 | 97 | 35 | 11 | 494 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
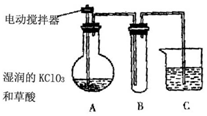 氯气或液氯消毒饮用水时,会和水中的有机物发生反应,生成对人体有毒的有机物.因此,世界环保联盟将全面禁止用氯气对饮用水消毒,建议推广采用安全、高效杀菌消毒剂ClO2.ClO2 是一种黄绿色、有刺激性气味的气体,熔点:-59.0℃,沸点:11.0℃,冷却至11.0℃以下时变成红色液体,易溶于水,见光易分解.ClO2易与NaOH反应,其杀菌、漂白能力均优于Cl2,消毒水体时不生成有害物质,也不存在用氯气消毒时残留的臭味.
氯气或液氯消毒饮用水时,会和水中的有机物发生反应,生成对人体有毒的有机物.因此,世界环保联盟将全面禁止用氯气对饮用水消毒,建议推广采用安全、高效杀菌消毒剂ClO2.ClO2 是一种黄绿色、有刺激性气味的气体,熔点:-59.0℃,沸点:11.0℃,冷却至11.0℃以下时变成红色液体,易溶于水,见光易分解.ClO2易与NaOH反应,其杀菌、漂白能力均优于Cl2,消毒水体时不生成有害物质,也不存在用氯气消毒时残留的臭味.查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | a>b>c | B. | b<a,b<c | C. | b>a,b>c | D. | a<b<c |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入足量氯化钙溶液 | 产生白色沉淀 | 溶液只有部分 |
| ②取少量充分反应后的溶液于试管中,滴入酚酞试液 | 酚酞试液变红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 20 克 | B. | 25 克 | C. | 30 克 | D. | 40 克 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com