
铁、铝、铜是常见的三种金属。同学们发现生活中的铝和铜制品表面一般不用防锈,而铁制品一般需要做防锈处理。
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
【实验探究】对这三种金属的活动性顺序探究,请你参与探究并 填写空格。
填写空格。
将粗细相同的铁丝、铝丝、铜丝分别插入体积相同、溶质质量分数也相同的稀盐酸中
| 操作 |
|
|
| 根据现象得出金属活动性顺序 |
| 片刻后现象 | 有少量气泡 | 无气泡 | 无气泡 | Fe>Al, Fe>Cu |
| 几分钟后现象 | 有少量气泡 | 有大量气泡 | 无气泡 |
【讨论交流】为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面致密的氧化膜会先与盐酸反应。
【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是 。
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中
| 操作 |
|
| 根据现象得出金属活动 |
| 现象 | 无明显现象 | Al>Fe>Cu |
写出铁与硫酸铜溶液反应的化学方程式 。
【拓展迁移】(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序。金属丝的插入顺序为 。
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜三种金属材料被人类利用的先后顺序 。
【解析】金属铝等容易被空气中的氧气氧化,所以,做金属性质实验时将金属进行打磨的目的是为了除去表面的氧化膜;铁和硫酸铜反应会生成铜和硫酸亚铁;将铜丝插入稀盐酸中没有现象,将铁丝插入稀盐酸中有气泡,说明铁的活动性大于铜,再插入铝丝,铝丝会和生成的氯化亚铁反应,说明铝的活动性大于铁;或者先将铁丝插入稀盐酸中生成氯化亚铁,再插入铜丝无现象,说明铁的活动性大于铜,再插入铝丝,会和氯化亚铁反应,说明铝的活动性大于铁;金属越活泼,被开发利用的就越晚。
答案:【实验探究】Al>Fe>Cu
【反思评价】除去金属表面的氧化物(或污物)
【实验验证】铁丝表面有红色物质析出,溶液由蓝色变为浅绿色 Fe+CuSO4====FeSO4+Cu
【拓展迁移】(1)Cu、Fe、Al(或Fe、Cu、Al)
(2)铜、铁、铝


科目:初中化学 来源: 题型:
学习了CO2的有关知识后,同学们查阅资料发现Mg能在CO2中燃烧:2Mg+CO2═2MgO+C,所以镁着火不能用CO2来灭火,但没有找到有关Na能否与CO2反应的介绍.于是同学们展开了钠着火能否用CO2来灭火的探究.
【提出猜想】钠能发生类似于CO2与镁的反应,可能的化学方程式为 _________ .
【实验】将燃着的钠伸入装有CO2的集气瓶中,钠能在集气瓶中继续燃烧.
进一步【查阅资料】得知:
①Na2O是白色固体,能与CO2反应生成Na2CO3,也能与H2O反应生成NaOH.
②Ba(OH)2溶于而BaCO3不溶于水.
③Na2CO3的存在会干扰NaOH的检测.
基于以上资料,同学们认为钠在CO2中燃烧的产物情况有所不同,并对产物提出了以下几种猜想:
Ⅰ.Na2O、C;Ⅱ _________ 、C;Ⅲ.NaOH、C;Ⅳ.Na2O、Na2CO3、C
通过理论分析,猜想 _________ (填序号)肯定错误的,理由是 _________
【验证猜想】
| 步骤 | 实验操作 | 主要实验现象 | 结论(燃烧产物判断) |
| (1) | 将产物溶于适量水中 | 部分溶解,试管底部有黑色固体 | 燃烧产物中肯定有C |
| (2) | 取少量(1)所得上层溶液,加入过量的BaCl2溶液 | _________ | 燃烧产物中肯定有Na2CO3 |
| (3) | 取少量(2)所得上层清液,加入 _________ 溶液 | 有蓝色沉淀生成 | 燃烧产物中肯定有 _________ |
在步骤(2)中BaCl2溶液为什么要加入至过量?其原因是: _________ .
【结论】猜想 _________ (填序号)是正确的.
查看答案和解析>>
科目:初中化学 来源: 题型:
下列有关金、银、铜三种金属的性质归纳中,正确的是 ( )
A.常温下三种金属颜色不同
B.都能和稀盐酸反应生成氢气
C.只用一种试剂不能区分三种金属的活动性强弱
D.金的金属活动性最强
查看答案和解析>>
科目:初中化学 来源: 题型:
请完成下面填空:
(1)性质决定用途。以下连线正确的是 (填字母)。

(2)用铁粉制成的食品保鲜剂使用一段时间后,会逐渐变为 色的氧化铁。
(3)用氯化物 (填化学式)溶液可以一次性验证Fe、Cu、Ag三种金属的活动性顺序。
查看答案和解析>>
科目:初中化学 来源: 题型:
二氧化硫是造成酸雨的主要物质之一。小丽为探究二氧化硫能与水反应生成酸,设计了如下实验方案。
【实验设计】她先用紫色石蕊溶液将白色滤纸浸润,干燥后做成紫色的小花,然后按下列图示进行实验。观察到实验(Ⅰ)和(Ⅲ)中的小花变红,(Ⅱ)中的小花不变色。
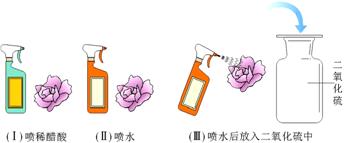
【评价反思】小虎对小丽的实验方案提出了质疑,他认为上述实验还不足以证明“二氧化硫和水反应生成了酸”。两位同学仔细讨论后认为还需补充如下一个实验,才能得出二氧化硫与水反应生成酸。
| 实验操作 | 实验现象 |
|
|
|
【拓展应用】二氧化硫也是实验室一种污染气体,常用碱液吸收。写出实验室用氢氧化钠溶液吸收二氧化硫的化学方程式: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
实验是学习化学的重要方法,在实验室里,常采取分解过氧化氢(H2O2)溶液的方法制取氧气.请分析图回答问题:
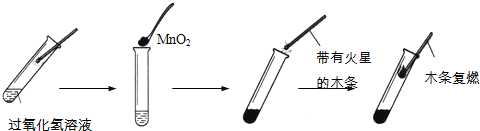
(1)MnO2在上述实验中所扮演的角色是 。
A.反应物B.生成物C.催化剂
(2) 图中能使带火星的木条复燃的气体是 。
图中能使带火星的木条复燃的气体是 。
(3)写出过氧化氢溶液快速分解的化学方程式 。
查看答案和解析>>
科目:初中化学 来源: 题型:
A.、B、C、D、E、F、G、H、I都是初中化学学过的物质。其中E、F、H均为黑色固体B为紫红色固体,D为混合物。他们之间有下图的转化关系(部分生成物已省去)
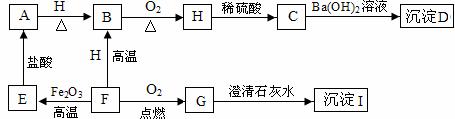
⑴用化学式表示:A ,I ,D的组成 、
⑵F→G的反应类型
⑶写出F→E的化学方程式
H→C的化学方程式
G→I的化学方程式
⑷指出B的一种用途
查看答案和解析>>
科目:初中化学 来源: 题型:
0.2%~0.5%的过氧乙酸[化学式(CH3COOOH)]溶液是一种杀菌能力强的高效消毒剂。
(1)过氧乙酸分子中C、H、O原子的个数比为________;
(2)欲配制0.4%的过氧乙酸溶液1000g,需用20%的过氧乙酸溶液_______克。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com