
 某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出2克合金样品,每次加入稀硫酸10克,共加入稀硫酸4次,充分反应后,过滤、洗涤、干燥、称重,得到的实验数据如图所示:
某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出2克合金样品,每次加入稀硫酸10克,共加入稀硫酸4次,充分反应后,过滤、洗涤、干燥、称重,得到的实验数据如图所示:分析 (1)因为铜不与硫酸反应,因此最后剩余的0.6g固体的成分是铜;从表格数据可知,每10g硫酸就消耗0.5g镁,所以第3次加入稀硫酸时样品中的镁已经完全反应;
(2)反应前后固体物质减少的质量为镁的质量,根据质量分数的计算公式可以求出镁铜合金中镁的质量分数;
(3)根据10g硫酸只能消耗0.5g镁进行计算,算出硫酸质量,再除以10g乘以百分之百即可
解答 解:(1)因为铜不与硫酸反应,因此最后剩余的0.6g固体的成分是铜;从表格数据可知,每10g硫酸就消耗0.5g镁,所以第3次加入稀硫酸时样品减少1g-0.6g=0.4g,说明样品中的镁已经完全反应;
故答案为:3;
(2)结合(1)的解答并分析题中数据可以知道第六次和第五次加入稀盐酸后金属的质量没有改变,所以可以判断铜的质量为0.6g,
所以镁的质量分数为=$\frac{2g-0.6g}{2g}$×100%=70%
故答案为:70%;
(3)设10克稀硫酸中所含H2SO4的质量为x.
Mg+H2SO4=MgSO4+H2↑
24 98
2g-1.5g x
$\frac{24}{2g-1.5g}=\frac{98}{x}$
x=2.04g
所用稀硫酸中溶质的质量分数:$\frac{2.04g}{10g}×100%$=20.4%
答:所用稀硫酸中溶质的质量分数为20.4%.
点评 本考点考查了表格型计算题,属于质量分数和化学方程式的综合应用,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,还要记牢“遇到差值要想气体”.本考点主要出现在计算题中.


 天天练口算系列答案
天天练口算系列答案科目:初中化学 来源: 题型:选择题
| A. | 碳酸钠溶液和稀盐酸反应Na2CO3+2HCl--NaCl+H2O+CO2复分解反应 | |
| B. | 用过氧化氢溶液和二氧化锰制氧气 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ 分解反应 | |
| C. | 用铁制容器盛放稀盐酸 2Fe+6HCl--2FeCl2+3H2↑置换反应 | |
| D. | 用熟石灰制生石灰 CaO+H2O--Ca(OH)2化合反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
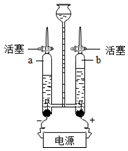 如图是水的电解实验装置图.
如图是水的电解实验装置图.| 时间/min 体积/mL | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 连电源负极的管(A)中气体 | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 |
| 连电源正极的管(B)中气体 | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧化物一定含有氧元素,含有氧元素的物质一定是氧化物 | |
| B. | 离子是带电荷的粒子,带电荷的粒子一定是离子 | |
| C. | 碱性溶液能使无色酚酞变红,能使无色酚酞变红的是碱性溶液 | |
| D. | 盐中含有金属离子和酸根离子,NH4NO3中不含金属离子,不属于盐类 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
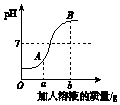
| A. | 该反应是稀HCl滴入NaOH溶液 | |
| B. | a g是指加入氢氧化钠固体的质量 | |
| C. | A点溶液的溶质为HCl和NaCl | |
| D. | 检验B点溶液的溶质可先滴加足量的MgCl2,静置后再滴加少量AgNO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com