
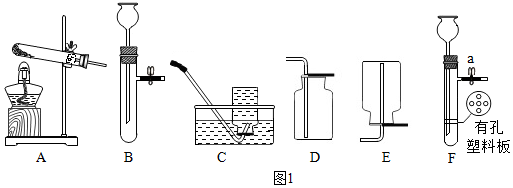
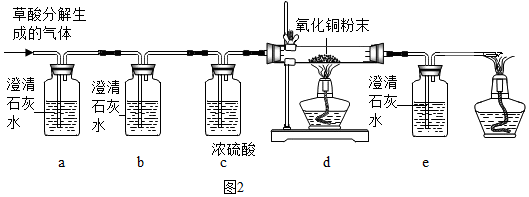
分析 (1)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,该反应的反应物是固体,反应条件是加热,氧气的密度比空气大,不易溶于水,二氧化碳不具有助燃性进行分析;
(2)根据实验室常用锌和稀硫酸反应生成制取氢气,反应过程中,关闭该装置中的止水夹a,装置内的压强增大进行分析;
(3)根据二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水进行分析;
(4)根据一氧化碳具有还原性,一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳进行分析;
(5)根据水蒸气不能干扰一氧化碳和氧化铜的反应现象,所以无需除去水蒸气进行分析;
(6)根据过滤可以将不溶性固体从溶液中分离出来,依据碳元素守恒进行分析;
(7)根据草酸在浓硫酸的催化作用下加热生成一氧化碳、二氧化碳和水进行分析.
解答 解:(1)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,该反应的反应物是固体,反应条件是加热,所以发生装置应选择A,氧气的密度比空气大,不易溶于水,所以收集装置应选择C或D,二氧化碳不具有助燃性,所以用装置D收集CO2,验满的方法是:把燃着的木条放在集气瓶口,木条熄灭,证明集满;
(2)实验室常用锌和稀硫酸反应生成制取氢气,铜片不会与酸反应生成氢气,浓盐酸具有挥发性,会使制取的氢气中因混有氯化氢气体而不纯净,所以用装置F制取H2,应选用的试剂是②③,反应过程中,关闭该装置中的止水夹a,装置内的压强增大,所以反应过程中,关闭该装置中的止水夹a,观察到的现象是:长颈漏斗中液面逐渐上升,固体和液体分离,装置F与装置B比较,其优点是:可以控制反应的发生和停止;
(3)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以实验过程中观察到装置a中的澄清石灰水变浑浊,证明有二氧化碳气体生成;
(4)一氧化碳具有还原性,一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,所以实验过程中还观察到装置b中澄清石灰水仍然澄清,装置e中有沉淀生成,装置d中黑色固体逐渐变成红色,证明有CO气体生成;
(5)水蒸气不能干扰一氧化碳和氧化铜的反应现象,所以无需除去水蒸气,所以实验过程中不需要装置c,理由是:水蒸气对一氧化碳的检验没有干扰;
(6)过滤可以将不溶性固体从溶液中分离出来,依据碳元素守恒,所以将a、e中的沉淀分别经过过滤、洗涤、干燥、称重,沉淀的质量相等,
假设生成的碳酸钙质量都是100g,设一氧化碳的质量为x,二氧化碳的质量为y
CO----CO2----CaCO3,
28 100
x 100g
$\frac{28}{x}$=$\frac{100}{100g}$
x=44g
CO2-----CaCO3,
44 100
y 100g
$\frac{44}{y}$=$\frac{100}{100g}$
y=44g
所以生成的二氧化碳和一氧化碳的质量比是44g:28g=11:7;
(7)草酸在浓硫酸的催化作用下加热生成一氧化碳、二氧化碳和水,化学方程式为:H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$CO2↑+CO↑+H2O.
故答案为:(1)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,A,C或D,把燃着的木条放在集气瓶口,木条熄灭,证明集满;
(2)②③,长颈漏斗中液面逐渐上升,固体和液体分离,可以控制反应的发生和停止;
(3)澄清石灰水变浑浊;
(4)黑色固体逐渐变成红色;
(5)水蒸气对一氧化碳的检验没有干扰;
(6)过滤,11:7;
(7)H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$CO2↑+CO↑+H2O.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:初中化学 来源: 题型:选择题
| A. | AgNO3溶液 | B. | Ba(OH)2溶液 | C. | NaOH溶液 | D. | 盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
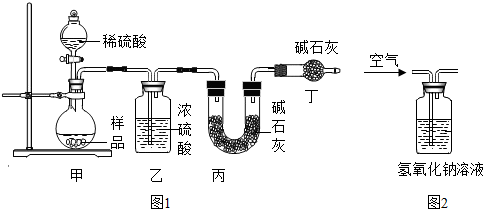

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
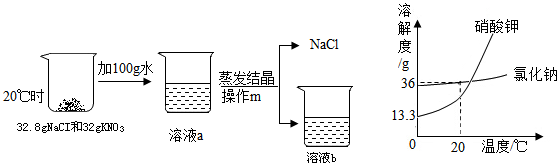
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
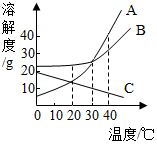 如图所示是A、B、C(均不含结晶水)三种物质的溶解度曲线,回答下列问题.
如图所示是A、B、C(均不含结晶水)三种物质的溶解度曲线,回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 喝了汽水会打嗝,说明压强减小气体的溶解度减小 | |
| B. | 住房失火,消防队员用水扑灭,是为了降低可燃性的着火点 | |
| C. | 常见的铁合金有生铁和钢,其中钢的含碳量较高 | |
| D. | 发现家中的燃气泄漏时,要立即关闭燃气阀门并打开门窗通风 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验方法 |
| A | 检验一瓶气体是否为二氧化碳 | 将燃着的木条伸入瓶中 |
| B | 鉴别石灰水和氢氧化钠溶液 | 加入适量的稀盐酸 |
| C | 比较三种金属活动性 | 将锌、银分别放入硝酸铜溶液中 |
| D | 鉴别聚乙烯和聚氯乙烯 | 点燃并在火焰山方各罩一烧杯观察 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com