
| A. | 羊毛衫 | B. | 塑料盆 | C. | 不锈钢餐具 | D. | 玻璃杯 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题

| A. | 向硫酸铜溶液中加入铁粉 | |
| B. | 向过氧化氢溶液中加入二氧化锰 | |
| C. | 向一杯接近饱和的石灰水中加入氧化钙 | |
| D. | 向不饱和的硝酸钾溶液中加入硝酸钾 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
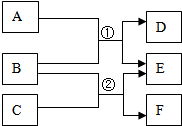 A-F表示初中化学常见的物质,A和B,B和C都能发生反应,且都只能生成两种产物,它们之间的转化关系如图所示.
A-F表示初中化学常见的物质,A和B,B和C都能发生反应,且都只能生成两种产物,它们之间的转化关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  加热氯酸钾和二氧化锰的混合物制取氧气 | |
| B. | 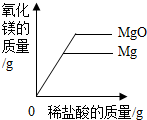 足量的氧化镁和镁与等质量、等质量分数的稀盐酸反应 | |
| C. |  相同质量的铁和铝分别与足量的稀硫酸反应 | |
| D. | 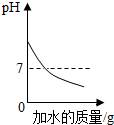 向一定量pH=13的氢氧化钠溶液中滴加大量的水 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
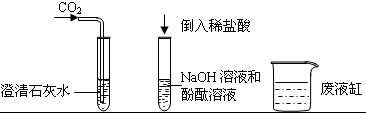
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 (
( 表示氧原子;
表示氧原子; 表示氢原子;
表示氢原子; 表示氯原子)
表示氯原子)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 时间h | 1 | 1.5 | 4 | 8 | 12 | 24 | 48 | 60 | |
| 吸水质量/g | 硫酸甲 | 1.6 | 2.2 | 5.2 | 10.3 | 14.0 | 20.9 | 29.2 | 32.1 |
| 硫酸乙 | 1.2 | 1.5 | 3.5 | 5.9 | 8.1 | 12.9 | 19.5 | 21.0 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com