
| 盐溶液 | NaCl | Na2CO3 | CaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样品溶于水配成溶液,向溶液中滴加CaCl2溶液至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中一定含有______(填化学式,下同). |
| ②用玻璃棒蘸取少量①的上层清液滴在pH试纸上,与标准比色卡对照. | pH=11 | 说明上述猜想中______是正确的. |


科目:初中化学 来源: 题型:
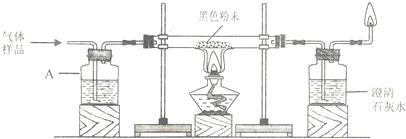
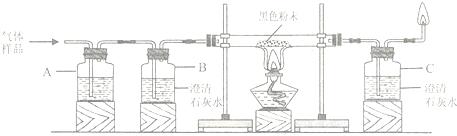
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| 试验操作 | 试验现象 | 试验结论 |
| (1)取少量固体于试管中,加适量水震荡后静置,再滴几滴无色酚酞试液 | 溶液变红 | 说明固体成分中一定含有 氧化钙(或CaO) 氧化钙(或CaO) |
| (2)再取少量固体于另一试管中滴加过量稀盐酸 | 有气泡生成 | 说明固体成分中一定含有 碳酸钙(或CaCO3) 碳酸钙(或CaCO3) |
查看答案和解析>>
科目:初中化学 来源: 题型:
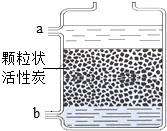 (2012?防城港)某校化学兴趣小组的同学对学校附近小河的水质状况进行了相关的调查研究.
(2012?防城港)某校化学兴趣小组的同学对学校附近小河的水质状况进行了相关的调查研究.查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com