
【题目】用如下图所示实验比较三种金属的活动性。

(1)若A为稀硫酸,实验观察到:①中有气泡产生,③中无明显变化,②中的现象为______。
(2)若A为硫酸铜溶液,实验观察到:①和②中金属表面均析出红色物质,③中无明显变化。写出②中发生反应的化学方程式______。
(3)上述实验可以证明金属活动性:B比______活泼。
科目:初中化学 来源: 题型:
【题目】科学家最近在-100℃的低温下合成一种化合物 X,此分子的模型如下图,其中每个![]() 代 表一个碳原子,每个
代 表一个碳原子,每个![]() 代表一个氢原子。下列说法中不正确的是
代表一个氢原子。下列说法中不正确的是

A.该分子的分子式为 C5H4
B.该分子中碳元素的质量分数是 93.75%
C.该物质中碳元素的化合价为+4 价
D.等质量的该物质与甲烷相比,燃烧时该物质消耗的氧气更多
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明将未打磨的铝片和稀盐酸放入密闭容器中,用传感器探究反应过程中温度和压强的变化,如右图所示。从图中所获信息不正确的是
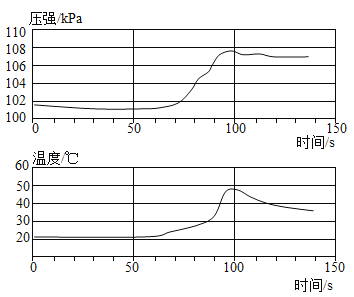

A. 反应过程中有热量放出B. 50s时,溶液中溶质为AlCl3
C. 0~50s,发生Al2O3+6HCl===2AlCl3+3H2O反应D. 100—140s,压强减小是因为温度降低
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】盐城盛产海盐。某化学兴趣小组同学在市场购到粗盐,带回实验室进行提纯。
①在溶解,过滤,蒸发等操作中,均用到的玻璃仪器是______(填仪器名称)。
②配制50g质量分數为6%的NaC1溶液,需称量NaCl固体_____g,若用粗盐配制上述解液,则所配溶液中NaCl的质量分数会_____(填“偏大”、偏小”或“无影响“)。
探究活动:以NaCl为原料可以制取金属钠。兴趣小组同学认为Na是活泼金属,能与CuSO4等盐溶液反应,生成相应的金属单质。
(提出问题)Na与CuSO4溶液反应,是否有Cu生成?
(设计实验)兴趣小组同学在老师的指导下,设计右图装置进行实验。

I.向大试管中加入一定体积煤油。
II.用小刀切一小块钠,放入大试管,塞上橡皮塞。
III.打开活塞,通过长颈漏斗向试管中加入CuSO4溶液。使煤油的液面升至胶塞,关闭活塞,观察现象。
(实验现象)
(1)Na在煤油与溶液交界处上下来回振动。表面产生气泡,逐渐变小直至消失。
(2)溶液颜色逐渐变淡,有蓝色絮状沉淀和少量黑色固体生成。
(3)打开活塞,用燃着的木条放在尖嘴管口处,气体被点燃。
(查阅资料)①Na通常存放在煤油中;②煤油不溶于水且不与水反应;
③2Na+2H2O=2NaOH+H2↑;④Cu(OH)2 △CuO+H2O。
(实验分析)
①根据上述信息,可获知金属钠的物理性质是_____(答出一点即可)。
(2)实验中长颈漏斗的作用________(填数字序号)。
①便于添加CuSO4溶液 ②收集气体 ③防止压强过大冲开活塞
(3)对于产生的气体,有些同学猜想是H2,有些同学猜想是SO2。小组同学经过讨论,排除了SO2,理由是________。经过进一步实验,确认气体是H2.
(4)将反应后的混合物过滤,向滤渣滴加足量稀硫酸,滤渣完全溶解。写出滤渣与稀硫酸反成的化学方程式________(写出一个即可)。
(实验结论)Na与CuSO4溶液反应,无Cu生成。
(实验反思)Na与CuSO4溶液无Cu生成,原因可能是_______。
(定量分析)另取一定量上述CuSO4溶液。完成下列实验。利用数据,计算无色溶液的溶质质量分数___________。(写出计算过程,滴入的酚酞溶液质量忽略不计。)

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了纪念伟大爱国诗人屈原,各地保留着不同的端午节习俗。

(1)赛龙舟。龙舟的不同部位选料考究,且精雕细琢上龙形图案。此过程中发生的变化属于__________ (填“物理”或“化学”)变化。
(2)吃粽子。用新鲜糯米、鲜牛肉为主料制作的鲜肉粽子中的主要营养成分有__________。
(3)熏艾。熏艾的简单方式是把艾草捆扎挂在门口或窗口,利用艾草的特殊气味驱赶蚊虫已达到防病目的。人能闻到艾草的气味是因为__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知:烧杯中的水均为100g,表是KC1、KNO3在不同温度时的溶解度。

温度 | 20℃ | 40℃ |
KC1 | 34.0g | 40.0g |
KNO3 | 31.6g | 63.9g |
①~④所得溶液属于饱和溶液的是
A.①B.②C.③D.④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
炭烧酸奶近年来发展迅速,其焦香浓郁的风味深受消费者喜爱。炭烧酸奶在制作过程中通过牛奶的长时间褐变,获得浓郁的焦香风味。牛奶褐变,是一系列化合物受热发生反应的过程。褐变生产工艺中需对葡萄糖用量、褐变温度和褐变时间三个重要条件进行严格控制。葡萄糖用量与产品颜色、风味密切相关,具体影响如图 2 所示,其中评分越高,产品的颜色、风味越好。褐变温度和时间的组合是调节蛋白稳定、避免沉淀分层的重要因素,具体影响如表所示,其中沉淀率越低产品越稳定。



表:褐变温度和时间对牛奶褐变沉淀率的影响
褐变温度/℃ | 86 | 88 | 90 | 92 | 94 | 96 |
褐变时间/h | 6 | 4 | 3.5 | 3 | 2.5 | 2 |
沉淀率/% | 0.35 | 0.31 | 0.27 | 0.22 | 0.14 | 0.44 |
优质的制作工艺可使炭烧酸奶口感爽滑,在保质期内状态稳定。依据文章内容回答下列问题。
(1)葡萄糖(C6H12O6)的相对分子质量是180,计算式为______。
(2)制作炭烧酸奶的原料有___________。
(3)牛奶褐变过程中,影响蛋白稳定的因素有_____________。
(4)由图表可知,牛奶褐变过程的最佳条件为_________。
(5)下列说法正确的是______(填序号)。
A 炭烧酸奶的特色是其浓郁的焦香风味
B 葡萄糖用量影响产品的颜色和风味
C 褐变温度越高,炭烧酸奶产品越稳定
D 炭烧酸奶制作过程中需将各种原料一次性混合均匀
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我们在选购包装(或罐装)食品时,“配料”一项中常常看到“山梨酸”或“山梨酸钾”的字样,山梨酸钾(C6H7KO2)在常温下是一种白色或微黄色粉末,易溶于水、乙醇.山梨酸钾是以山梨酸(C6H8O2)和碳酸钾或氢氧化钾为原料,在经过化学反应后制作而成.山梨酸及山梨酸钾是国际粮农组织推荐的高效安全的防腐保鲜剂,广泛应用于食品、饮料、烟草、农药、化妆品等行业.
(1)22.4g山梨酸中含氧元素的质量是_________g.
(2)请写出山梨酸与氢氧化钾发生中和反应生成山梨酸钾的化学方程式:_____________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法正确的是( )

A.t1℃时,相同质量的甲、丙溶液中溶质质量一定相同
B.若甲物质中含有少量乙,可用降温结晶的方法提纯甲
C.将100g甲的饱和溶液从t2C降温到t1℃,可析出30g甲物质
D.将甲、乙、丙三种物质的饱和溶液从t2℃降温到t1℃,所得溶液的溶质质量分数由大到小的顺序为乙>甲=丙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com