
| 实验步骤 | 实验现象 | 反应的化学方程式 |
| ①往滴有石蕊试液的NaOH溶液中逐滴加入稀盐酸,并不断搅拌,至盐酸过量. | 溶液蓝色逐渐变浅至紫色,然后变为红色 |
NaOH+HCl=NaCl+H2O |
| ②往滴有酚酞试液的NaOH中逐滴加入适量的CuCl2溶液,然后静置一段时间. | 溶液红色逐渐消失,有蓝色沉淀生成 |
CuCl2+2NaOH=Cu(OH)2↓+2NaCl |
| ③往滴有酚酞试液的Ba(OH)2中逐滴加入适量的Na2CO3溶液,然后静置一段时间. | 溶液不变色,有白色沉淀生成 |
Ba(OH)2+Na2CO3=BaCO3↓+2NaOH |
| 实验步骤 | 实验现象 | 反应的化学方程式 |
| 溶液蓝色逐渐变浅至紫色,然后变为红色 | NaOH+HCl=NaCl+H2O | |
| 溶液红色逐渐消失,有蓝色沉淀生成 | CuCl2+2NaOH=Cu(OH)2↓+2NaCl | |
| 溶液不变色,有白色沉淀生成 | Ba(OH)2+Na2CO3=BaCO3↓+2NaOH |


科目:初中化学 来源: 题型:阅读理解
| 白色粉末的成分 | 形 成 的 原 因 |
| 可能是CaCO3 | 石灰水与空气中CO2反应: 化学方程式为: CO2+Ca(OH)2═CaCO3↓+H2O |
| 可能是 氢氧化钙 |
暑假气温较高,溶质的溶解度降低或溶剂蒸发,石灰水中的溶质析出 |
| OH- | Cl- | CO32- | NO3- | |
| Ca2+ | 微 | 溶 | 不 | 溶 |
| 实 验 步 骤 | 可能观察到的现象 | 结 论 |
| 取上述试管中的上层清液,滴加1~2滴无色酚酞试液 | 溶液变红 |
固体中含有氢氧化钙 |
| 往上述试管内残留的固体中加入稀盐酸 | 产生气泡 |
白色粉末中 有 (“有”或“无”)CaCO3 |
| 由上述实验可知白色粉末的成分是: 碳酸钙和氢氧化钙的混合物 | ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 溶液 | A | B | C |
| 加入盐酸后的现象 | 无明显变化 | 无明显变化 | 有气泡产生 |
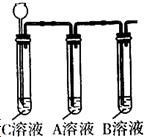
| 实验步骤 | 实验现象 | 结论 |
| 取A、B两溶液分别于两支试管中,各滴加C溶液 | 该溶液是A 溶液 | |
| 该溶液是B溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2012?延庆县二模)根据如图所示的实验回答问题.
(2012?延庆县二模)根据如图所示的实验回答问题.| 实验操作 | 实验现象 | 实验结论 |
| a. 观察试管③溶液颜色 观察试管③溶液颜色 .b.若试管③溶液为无色,取无色溶液少量于一支试管中,向其中加入 碳酸钠溶液 碳酸钠溶液 . |
若试管③溶液为红色 若无气泡产生 若无气泡产生 .若有气泡产生 若有气泡产生 . |
试管③溶液中的溶质是: NaCl、NaOH NaCl、NaOH .试管③溶液中的溶质是:NaCl. 试管③溶液中的溶质是: NaCl、HCl NaCl、HCl . |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象及结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 步骤 | 现象 | 分析 |
| (1)点燃“果冻蜡烛”,并在火焰上方罩一个干燥而冷的小烧杯 | 烧杯内壁有无色小液滴生成 | “果冻蜡烛”燃烧后的产物有 水 水 |
| (2)迅速倒转小烧杯,向其中加入适量 澄清石灰水 澄清石灰水 ,振荡 |
澄清石灰水变浑浊 澄清石灰水变浑浊 |
“果冻蜡烛”燃烧后的产物有二氧化碳 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com