
分析 氧化铜和稀硫酸反应生成硫酸铜和水,根据杂质的质量可以计算氧化铜的质量;
根据氧化铜的质量可以计算反应生成硫酸铜的质量,进一步可以计算反应后溶液中溶质的质量分数.
解答 解:①样品中氧化铜的质量为9.6g-1.6g=8g,
答:样品中氧化铜的质量是8g.
②设反应生成CuSO4的质量为x,
CuO+H2SO4═CuSO4+H2O,
80 160
8g x
$\frac{80}{8g}$=$\frac{160}{x}$,
x=16g,
反应后溶液中溶质硫酸铜的质量分数为:$\frac{16g}{8g+92g}$×100%=16%,
答:反应后溶液中溶质硫酸铜的质量分数为16%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 金属导电--原子是运动的 | |
| B. | 夏天钢轨之间的缝隙变小--原子之间有间隔 | |
| C. | 氮气的化学性质不如氧气活泼--不同分子性质不同 | |
| D. | 电解水实验--分子在化学反应中可以再分 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题

| A. | MgCl2、HNO3、K2SO4 | B. | BaCl2、HNO3、K2SO4 | ||
| C. | NaNO3、H2SO4、Ba(NO3)2 | D. | CaCl2、HCl、AgNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 实验操作 | 实验现象 | 实验结论 |
| 漂白液已经失效 |
| 实验操作及实验现象 | 实验现象 | 实验目的或预期结论 |
| 步骤①;取少量该漂白液于试管中,加入足量的CaCl2溶液,静置,观察 | 产生白色沉淀 | 目的:除去Na2CO3 |
| 步骤②:取上层清液于试管中, 滴入无色酚酞试液,观察 | 试液变红(或试液无明显变化) | 结论:③(或②)猜想成立;否则,另一位同学猜想成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 杂质 | 除杂质选用的试剂和操作方法 | |
| A | CO2 | CO | 通入O2,点燃 |
| B | CO2 | HCl气体 | 通入氢氧化钠溶液,再通过浓硫酸 |
| C | NaCl溶液 | Na2CO3溶液 | 加入稀硫酸至不再产生气泡为止 |
| D | 碳酸钙 | 氯化钙 | 加入足量的水溶解,过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
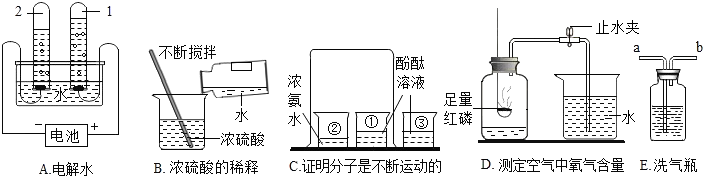
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com