


| 溶解度 |
| 溶解度+100g |
| 溶解度 |
| 溶解度+100g |
| 100g |
| 200g |
| 溶解度 |
| 溶解度+100g |
| 溶解度 |
| 溶解度+100g |


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:初中化学 来源: 题型:
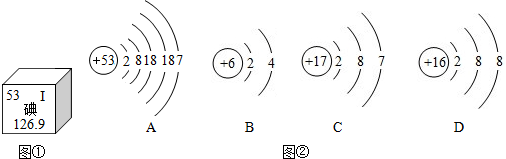
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
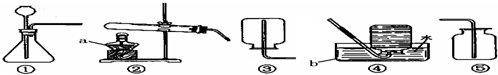
查看答案和解析>>
科目:初中化学 来源: 题型:
| 错误说法 | 否定错误说法的事实 |
| (1)混合后有白色沉淀生成的两种无色溶液一定分别是硫酸和氯化钡溶液 | |
| (2)中和反应都没有明显现象 | |
查看答案和解析>>
科目:初中化学 来源: 题型:
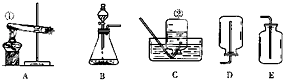
查看答案和解析>>
科目:初中化学 来源: 题型:
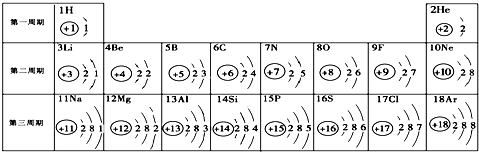
| 物质的类别 | 单质 | 氧化物 |
| 物质的化学式 |
查看答案和解析>>
科目:初中化学 来源: 题型:
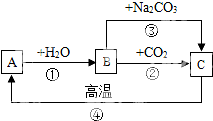
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com