

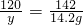
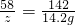
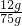 ×100%=16%
×100%=16% 

 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:初中化学 来源: 题型:

| 蒸发皿的质量 | 蒸发皿的质量+食盐溶液的质量 | 蒸发皿的质量+食盐晶体的质量 |
| 28.8克 | 48.8克 | 30.7克 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 某公司生产出的纯碱产品中经检测只含有氯化钠杂质.为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示.
某公司生产出的纯碱产品中经检测只含有氯化钠杂质.为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:
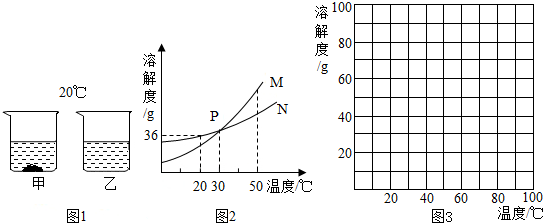
| 温度(℃) | 0 | 10 | 20 | 40 | 50 | 60 | 70 |
| KNO3 | 13.3 | 20.9 | 31.6 | 64 | 85.5 | 110 | 138 |
| NaCl | 35.7 | 35.8 | 36 | 36.6 | 37 | 37.5 | 37.8 |
查看答案和解析>>
科目:初中化学 来源:2013年山东省济南市中考化学模拟试卷(一)(解析版) 题型:解答题

| 蒸发皿的质量 | 蒸发皿的质量+食盐溶液的质量 | 蒸发皿的质量+食盐晶体的质量 |
| 28.8克 | 48.8克 | 30.7克 |
查看答案和解析>>
科目:初中化学 来源:2012年浙江省衢州市中考化学试卷(解析版) 题型:解答题
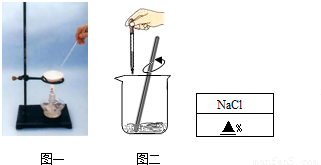
| 蒸发皿的质量 | 蒸发皿的质量+食盐溶液的质量 | 蒸发皿的质量+食盐晶体的质量 |
| 28.8克 | 48.8克 | 30.7克 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com