
已知氯磺酸化学式为ClSO3H,能在水中完全电离出H+和ClSO3﹣;甲酸化学式为HCOOH,能在水中部分电离出H+和HCOO﹣.对于反应C1SO3H+HCOOH═CO↑+HCl+H2SO4有如下判断,其中合理的是( )
|
| A. | 此反应属于复分解反应 | B. | 此反应中碳元素的化合价发生改变 |
|
| C. | 反应前后溶液的总质量不变 | D. | 反应后溶液的pH减小 |
| 酸的化学性质;溶液的酸碱性与pH值的关系;有关元素化合价的计算;反应类型的判定.. | |
| 专题: | 常见的酸 酸的通性. |
| 分析: | A、复分解反应是两种化合物相互交换成分生成两种新的化合物的反应. B、根据化合价原则来判断分析反应前后碳元素的化合价. C、根据质量守恒定律,进行分析判断. D、根据反应物与生成物的酸碱性来判断溶液pH值的变化. |
| 解答: | 解:A、由反应C1SO3H+HCOOH═CO↑+HCl+H2SO4,该反应不是两种化合物相互交换成分生成两种新的化合物的反应,不属于复分解反应,故选项说法错误. B、HCOOH分子是由H+和COOH﹣构成,可以设在本化合物中碳元素的化合价x,则(+1)+x+(﹣2)×2+(+1)=0,所以x=+2,而一氧化碳中碳元素的化合价为+2价,在该反应中碳元素的化合价没有发生改变,故选项说法错误. C、由质量守恒定律,反应后一氧化碳逸出,反应后溶液的总质量减少,故选项说法错误. D、反应前甲酸能在水中部分电离出H+和HCOO﹣,说明HCOOH的酸性较弱,而反应后生成的盐酸和硫酸都是强酸,反应后溶液的酸性要强于反应前的溶液的酸性,溶液的pH值要减小,故选项说法正确. 故选:D. |
| 点评: | 本题难度不大,掌握酸的化学性质、复分解反应的特征、化合价的原则、溶液的酸碱性和溶液pH大小之间的关系是正确解答本题的关键. |


科目:初中化学 来源: 题型:
如图所示:淀粉水解可产生某有机化合物A,A在 不同氧化剂的作用下,可以生成B(C6H12O7)或
不同氧化剂的作用下,可以生成B(C6H12O7)或
C(C6H10O8),B和C都不能发生银镜反应。A、B、C都可以被强还原剂还原为D(C6H14O6)。B脱水可得到
五元环的酯类化合物E或六元环的酯类化合物F。已知,相关物质被氧化的难易次序是RCHO最易,
R—CH2OH次之, 最难。
最难。
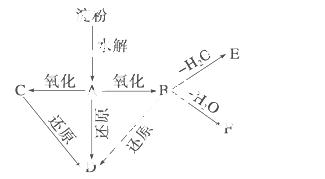
请在下列空格中填写A、B、C、D、E、F的结构简式。
A:________________________,B:____________________________________,
C:________________________,D:____________________________________,
E:________________________,F:____________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
分类是学化学的方法之一,下列物质是按氧化物、盐、混合物顺序排列的是( )
|
| A. | 蒸馏水、大理石、澄清石灰水 | B. | 酒精、硫酸钠、泥浆水 |
|
| C. | 氧化铜、高锰酸钾、冰水混合物 | D. | 干冰、碳酸钙、空气 |
查看答案和解析>>
科目:初中化学 来源: 题型:
2012年6月18日神舟九号飞船与天宫一号目标飞行器实现自动交会对接,这是中国实施的首次载人空间交会对接.天宫一号目标飞行器内镍氢电池的总反应式H2+2NiO(OH)=2Ni(OH)2,下列叙述不正确的是( )
|
| A. | H2是单质 |
|
| B. | NiO(OH)2是氧化物 |
|
| C. | 参加反应的H2、NiO(OH)的质量比为1:92 |
|
| D. | 在阴影区的时候,由电池来给飞船进行供电,将化学能转化为电能 |
查看答案和解析>>
科目:初中化学 来源: 题型:
现有铁、氧化铁、稀硫酸、氢氧化钙、碳酸钠溶液等五种物质,存在着如图所示的相互反应或转化关系(图中“﹣”表示物质间可以发生化学反应,“→”表示物质间存在相应的转化关系).下列判断合理的是( )
|
| A. | 丙可能是碳酸钠溶液 | B. | 丁可能是氢氧化钙溶液 |
|
| C. | 乙必须通过置换反应转化为铁 | D. | 甲和丁的反应一定是中和反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:
我国化工专家侯德榜曾为世界制碱工业作出了突出贡献.“侯氏制碱法”是
食盐、氨气、二氧化碳等为原料先制得NaHCO3,进而生产出纯碱.其生产过程用化学方程式可简要表示为:
①NH3+CO2+H2O=NH4HCO3②NH4HCO3+NaCl=NaHCO3↓+NH4Cl
③2NaHCO3 Na2CO3+H2O+CO2↑ NH4HCO3
Na2CO3+H2O+CO2↑ NH4HCO3 NH3↑+H2O+CO2↑
NH3↑+H2O+CO2↑
(1)“侯氏制碱法”生产过程中没有涉及到的基本反应类型是 .
A.置换反应 B.化合反应 C.分解反应 D.复分解反应
(2)若第②步中得到的NaHCO3中含有少量的NH4HCO3.但不会影响产品Na2CO3的纯度,原因是 .
(3)若纯碱中含有NaHCO3杂质,为测定试样中纯碱的质量分数,用如图中的装置进行实验.主要实验步骤如下:用天平准确称量出干燥试管的质量为20.2克,然后称取4.0克已研碎的纯碱样品并放入干燥的试管中.用酒精灯加热,待充分反应并冷却后,在天平上称出试管和碳酸钠的质量23.5克.该试样中纯碱的质量分数为 .(保留一位小数)
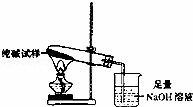
查看答案和解析>>
科目:初中化学 来源: 题型:
下列关于科学实验中“操作-现象-结论”的描述正确的是(▲)
A、在某固体物质中加入稀盐酸,产生大量气泡,该物质一定是碳酸盐
B、在某溶液中加入氯化钡溶液和稀硝酸,产生白色沉淀,该溶液中一定含有硫酸根离子
C、某化肥与碱共热,若产生使湿润红色石蕊试纸变蓝的气体,证明为铵态氮肥
D、在稀盐酸与氢氧化钠反应后的溶液中滴加无色酚酞试液不变色,可以断定两者恰好完全反应
查看答案和解析>>
科目:初中化学 来源: 题型:
某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加稀硫酸反应,将得到的实验数据绘制出如图象:其实验数据记录如下表.
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
试回答:
(1)经分析,在第1份样品测得的数据中, (填物质)完全反应了.
(2)列式计算黄铜屑样品中的锌的质量分数.
(3)所用稀硫酸中溶质的质量分数.

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com