
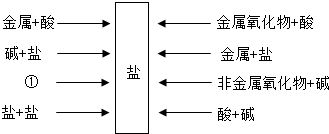

分析 (1)根据酸和盐反应也会生成新酸和新盐进行分析;
(2)根据硬水中含有较多可溶性钙镁化合物,氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠进行分析;
(3)①根据操作Ⅰ、Ⅱ、Ⅲ都是将固体和溶液分离,以及过滤需要需要的仪器,结合题中除去的杂质进行分析;
②根据题中除杂过程中加入的氢氧化钠、碳酸钠都是过量的,对于氯化钠来说也是杂质进行分析;
③根据操作Ⅳ是从氯化钠溶液中得到氯化钠晶体进行分析;
(4)根据氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,依据题中的数据进行计算.
解答 解:(1)酸和盐反应也会生成新酸和新盐,所以图中①处反应物是酸+盐;
(2)硬水中含有较多可溶性钙镁化合物,所以硬水中含有较多的Ca2+、Mg2+化合物,氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,化学方程式为:2NaOH+MgCl2═Mg(OH)2↓+2NaCl;
(3)①操作Ⅰ、Ⅱ、Ⅲ都是将固体和溶液分离,所以该操作是过滤,过滤需要需要的仪器有烧杯、漏斗、玻璃棒,加入过量的G是除去氯化钙,所以固体F中的物质有碳酸钙;
②题中除杂过程中加入的氢氧化钠、碳酸钠都是过量的,对于氯化钠来说也是杂质,所以图中加入过量的试剂的目的是除去反应剩余的碳酸钠和氢氧化钠;
③操作Ⅳ是从氯化钠溶液中得到氯化钠晶体,所以操作Ⅳ中除去了水和过量的稀盐酸;
(4)设参加反应的氢氧化钠的质量为x
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,
160 80
40g×10% x
$\frac{160}{80}$=$\frac{40g×10%}{x}$
x=2g
故答案为:(1)酸+盐;
(2)Ca2+、Mg2+,2NaOH+MgCl2═Mg(OH)2↓+2NaCl;
(3)①过滤,烧杯、漏斗、玻璃棒,碳酸钙;
②除去反应剩余的碳酸钠和氢氧化钠;
③水和过量的稀盐酸;
(4)参加反应的氢氧化钠的质量为2g.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的提示进行解答.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
 A~D是初中化学中常见物质,且有如图所示的转化关系(反应条件、部分反应和生成物均已略去),请按照要求回答:
A~D是初中化学中常见物质,且有如图所示的转化关系(反应条件、部分反应和生成物均已略去),请按照要求回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
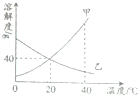 如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )| A. | 20℃时,甲、乙两物质的溶解度相等 | |
| B. | 升高温度可以将乙的饱和溶液变为不饱和溶液 | |
| C. | 40℃时,将40g甲放入100g水中可得到饱和溶液 | |
| D. | 10℃时,分别用100g水配制甲、乙的饱和溶液,所需甲的质量大于乙的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
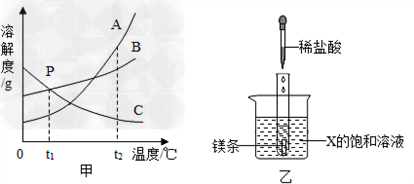
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一个分子中含有7个原子 | B. | 尿素由三种元素组成 | ||
| C. | 碳元素和氧元素的质量之比是1:1 | D. | 氮元素的质量分数约为46.7% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com