
分析 (1)根据题中的叙述找出反应物、生成物,根据方程式的书写规则进行书写方程式,氢氧化钙和盐酸反应生成了氯化钙和水;根据反应的程度进行猜想:恰好反应、一种物质完全反应,另一种物质有剩余;
(3)氢氧化钙溶液显碱性,能使酚酞试液变红色;
(4)碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳,能和氯化钙反应生成碳酸钙沉淀和氯化钠;
(5)显碱性的溶液能使石蕊试液变蓝色,显酸性的溶液能使石蕊试液变红色,显中性的溶液不能使石蕊试液变色;
【反思拓展】从反应进行的程度考虑.
解答 解:(1)氢氧化钙和盐酸发生中和反应生成氯化钙和水,故该反应的化学方程式为:Ca(OH)2+2HCl═CaCl2+2H2O;
【提出猜想】溶质可能是CaCl2和Ca(OH)2,也可能是CaCl2,也可能是CaCl2和HCl.
(3)取少量上述实验中烧杯里的溶液于试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到溶液不变色.于是可以确定“猜想一”不成立”,其理由是如果含有氢氧化钙,则酚酞试液变红色;
(4)取少量上述实验中烧杯里的溶液于试管中,并向试管中逐滴加入过量的碳酸钠溶液,先出现气泡,说明溶液中含有HCl,后有白色沉淀生成,说明溶液中含有氯化钙,于是可以确定猜想三成立.
(5)向上述实验中烧杯里的溶液中滴加适量的石蕊试液,如果溶液变红色,说明溶质是氯化钙和氢氧化钙;
如果溶液不变色,说明溶质是氯化钙;
如果溶液变红色,说明溶质是氯化钙和氯化氢.
【反思拓展】在分析化学反应后所得物质的成分时不仅考虑生成物有什么,还需要考虑反应物中什么物质过量问题,谁过量就含有谁.
故答案为:(1)Ca(OH)2+2HCl═CaCl2+2H2O;HCl;
(3)不成立;如果含有氢氧化钙,则酚酞试液变红色;(4)白色沉淀;猜想三(5)B;(6)反应物是否有剩余.
点评 本题考查了酸碱中和反应以及实验设计的能力.设计实验时,可以从反应后的产物和其有关的性质着手.


科目:初中化学 来源: 题型:选择题

| A. | 如图①所示用湿润的pH试纸测定稀盐酸的酸碱度,会使pH偏下 | |
| B. | 实验室用NH4Cl和Ca(OH)2的固体混合物加热制氨气,选用图②装置 | |
| C. | 如图③所示配制50g 20%的蔗糖溶液,会使溶质质量分数偏小 | |
| D. | 图④将水沿烧杯壁缓缓倒入浓硫酸中边到边搅进行稀释 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在做“粗盐中难溶性杂质的去除”实验时,玻璃棒用了四次 | |
| B. | 能与盐酸反应产生气体的固体物质一定是碳酸盐 | |
| C. | 沉淀过程中一定伴随着化学反应 | |
| D. | 能使无色酚酞溶液变红的物质一定是碱 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
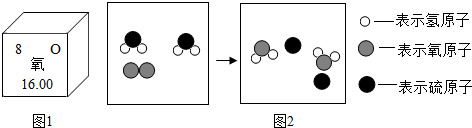
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
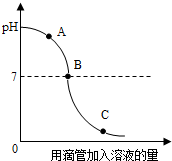 实验小组探究稀盐酸和氢氧化钠溶液反应过程中溶液pH的变化规律,得到如图所示曲线,下列有关该实验事实的说法正确的是( )
实验小组探究稀盐酸和氢氧化钠溶液反应过程中溶液pH的变化规律,得到如图所示曲线,下列有关该实验事实的说法正确的是( )| A. | A点时的溶液不能使酚酞溶液变色 | |
| B. | B点表示稀盐酸和氢氧化钠溶液恰好完全反应 | |
| C. | C点时,溶液中溶质只有氯化氢 | |
| D. | 该实验是将氢氧化钠溶液滴入稀盐酸中 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 没有腐蚀性的药品可以直接放在电子秤上称量,具有腐蚀性的应放在烧杯中称量 | |
| B. | 测定某溶液的pH值,将pH试纸浸入待测溶液中,后与标准比色卡比较确定 | |
| C. | 实验完毕后,实验过程中剩余的试剂都应放回原试剂瓶,不得乱扔乱倒 | |
| D. | 烧杯加热时应放置在石棉网上进行 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 50% | B. | 20% | C. | 10% | D. | 40.8% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com