
| 选项 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
| A | 10mLCO2 | 10mL浓氢氧化钠溶液 | 活塞自动向内压缩 |
| B | 20mLH2 | 10mLO2 | 生成无色液体,活塞自动向内压缩 |
| C | 10mLFe2(SO4)3溶液 | 10mLBa(OH)2溶液 | 生成白色沉淀 |
| D | 1g铁粉末 | 10mL49%密度为1.3g/mL稀硫酸 | 生成无色气体,溶液呈浅绿色,活塞自动外移,无固体剩余 |
| A.A | B.B | C.C | D.D |
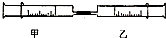
| 56 |
| 98 |
| 1g |
| X |


科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:
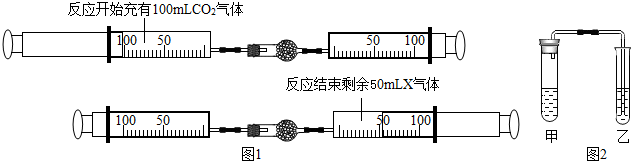
| 操作 | 现象 | 化学方程式 |
| 甲中加入白色物质Y,乙中加入 ③ ③ (填试剂序号,下同),再向甲中加入① ① . |
甲中产生气泡;乙中产生白色沉淀. | 甲中 Na2CO3+H2SO4═Na2SO4+H2O+CO2↑ Na2CO3+H2SO4═Na2SO4+H2O+CO2↑ ;乙中 Ca(OH)2+CO2═CaCO3↓+H2O Ca(OH)2+CO2═CaCO3↓+H2O . |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
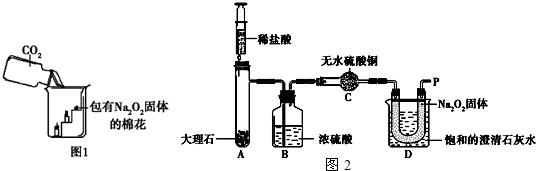
过氧化钠(Na2O2)是一种淡黄色固体。在一次科技活动中,同学们将包有Na2O2固体的棉花放入了如右图所示的装置中,发现高低不同的两根蜡烛,下面的蜡烛先熄灭,上面的蜡烛后熄灭,同时也惊奇地发现棉花燃烧了起来。
(1)实验过程中蜡烛由下往上依次熄灭,说明二氧化碳
具有 的性质。
(2)棉花为什么会燃烧呢?同学们认为棉花要燃烧,除了满足棉花是可燃物之外,还需
满足 、  。
。
【提出问题】上述实验中是如何给棉花提供燃烧条件的?
【查阅资料】1.在常温下Na2O2与CO2、H2O均能发生化学反应。
2.无水硫酸铜为白色固体,吸水后变为蓝色。
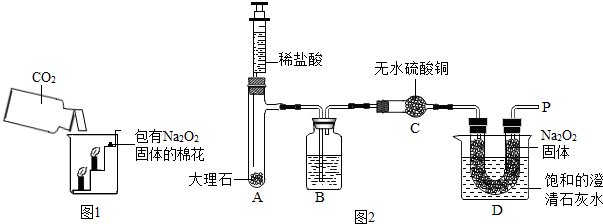
【实验设计】经过讨论,同学们设计用下图所示装置进行实验探究。
 | |||
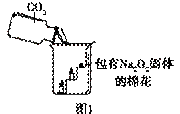 | |||
【实验步骤】①检查整套装置的气密性; ②把相关的试剂放入对应的仪器内;
③用力推动针筒的活塞,把稀盐酸注入试管内;
④一段时间后,在P处放 置一根带火星的木条,观察现
置一根带火星的木条,观察现 象。
象。
注意:大理石与稀盐酸制取的CO2还会含有一定量的水蒸气,但整个实验过程中不考虑稀盐酸的挥发和空气对实验的影响。
【实验现象】
①带火星的木条复燃; ②无水硫酸铜没有变蓝色; ③饱和的澄清石灰水变浑浊。
【实验分析】①B装置内盛放的试剂是 ;②D装置烧杯内澄清石灰水变浑浊的原因可能是 ,也可能是空气中的CO2与澄清石灰水反应生成了难溶物使澄清石灰水变混浊。
【实 验结论】
验结论】 ①Na2O2和CO2反应产生的一种气体,使图1中的棉花满足了燃烧的一个条件。
①Na2O2和CO2反应产生的一种气体,使图1中的棉花满足了燃烧的一个条件。
②Na2O2和CO2反应过程中伴随能量变化,使图1中的棉花满足了燃烧的另一个条件。
【拓展提高】①Na2O2和CO2反应除生成一种气体外,还生成了一种固体,学生甲认为生成的固体是NaOH,学生乙认为是Na2CO3,同学们经思考后认为甲同学的猜想是错误的,理由是 。
②写出Na2O2和CO2反应的化学方程式  。
。
【定量探究】有一包久置的过氧化钠粉末,现已证明因其保存不当导致完全变质成为NaOH和Na2CO3的混合物,同学们称取了13.25g样品,加入足量稀盐酸,并将产生的气体通入足量的澄清石灰水中,得到白色沉淀,经过滤、洗涤、烘干后称得其质量为10g,试计算:样品中Na2CO3的质量分数。
查看答案和解析>>
科目:初中化学 来源:2013年江苏省南京市高淳县中考化学一模试卷(解析版) 题型:填空题
| 操作 | 现象 | 化学方程式 |
| 甲中加入白色物质Y,乙中加入 (填试剂序号,下同),再向甲中加入 . | 甲中产生气泡;乙中产生白色沉淀. | 甲中 ; 乙中 . |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com