
| 成分 | 所用物质 |
| 碳酸盐类 | 碳酸氢钠 |
| 酸性物质 | 柠檬酸、酒石酸等 |
| 疏松剂 | 明矾 |
| 其他成分 | 淀粉、脂肪酸等 |

分析 碳酸钠和碳酸氢钠是食品工业常用的试剂,这两种物质热稳定性不同,但是都显碱性,都能与酸反应生成二氧化碳气体,碳酸氢铵中含有的铵根离子与碱性物质混合会生成有刺激性气味的氨气,含有的碳酸氢根离子与酸结合能生成二氧化碳气体.
解答 解:实验一:(2)碳酸氢钠能与盐酸反应生成氯化钠、二氧化碳和水,所以本题答案为:NaHCO3+HCl═NaCl+H2O+CO2↑;
(3)①导管伸入液体中,给加热试管结束后,为防止液体倒吸使试管炸裂,需要先将导管移出,再熄灭酒精灯,所以本题答案为:先将烧杯a、b中的导气管移出,再熄灭酒精灯;
②大试管内放的是碳酸钠,a烧杯中石灰水无明显现象,说明碳酸钠受热不分解,小试管内放的是碳酸氢钠,加热后无水硫酸铜变蓝,说明有水生成,b烧杯中石灰水了现白色浑浊,说明有二氧化碳生成,从而说明碳酸氢钠受热易分解,面团发酵能产生酸,用碱面蒸馒头,可以使面团发酵产生的酸与碳酸钠反应生成二氧化碳,所以本题答案为:碳酸钠受热不分解,碳酸氢钠受热分解出水和CO2等物质;使碱面与酸反应生成CO2气体(碳酸钠受热不分解).
实验二:①该物质能与酸反应生成二氧化碳气体,且受热易分解,说明该物质中含碳酸氢根离子,与碱性物质混合能产生了使湿润的红色石蕊试纸变蓝的臭气,说明该物质中含有铵根离子,故该物质为碳酸氢铵,所以本题答案为:NH4HCO3;NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑;
②“臭粉”作疏松剂来油炸食品会产生有刺激性气味的氨气,所以要放置一段时间,使产生的氨气挥发掉,所以本题答案为:使煎炸产生的氨气挥发;
③碳酸氢铵中碳酸氢根的含量比碳酸氢钠中碳酸氢根的含量高,如果两种物质的质量相同,碳酸氢铵生成气体的量比碳酸氢钠多,所以本题答案为:等质量的碳酸氢铵生成气体的量比碳酸氢钠多.
实验三:
(1)小苏打、“臭粉”中都含有碳酸氢根离子,具有相似的性质,都能与酸反应生成二氧化碳,都不稳定,受热易分解,所以本题答案为:CO2;受热分解出二氧化碳;与酸反应产生二氧化碳;
(2)用将少许面粉加入水中取上层液体用pH试纸测得:pH=7,说明溶液呈中性,应该是受热分解产生了二氧化碳,所以本题答案为:受热分解出的二氧化碳.
实验四:
(1)该疏松剂中含碳酸氢钠和某些酸类物质,所以使用后会生成二氧化碳,根据碳酸氢钠的性质,可知产生二氧化碳的途径可以是与酸反应,也可以是受热分解,所以本题答案为:CO2;受热分解出二氧化碳;与酸反应产生二氧化碳;
(2)①要测定二氧化碳的质量,必须保证装置不漏气,所以进行实验前要检查装置的气密性,使疏松剂产生二氧化碳可加入稀硫酸,如果加入盐酸会使二氧化碳中混有氯化氢气体,所以本题答案为:装置的气密性;稀硫酸;
②乙装置盛的浓硫酸具有吸水性,故可用来干燥二氧化碳,甲装置盛的是氢氧化钠溶液,可以吸收空气中的二氧化碳,防止测定的数据不准确,所以本题答案为:吸收二氧化碳中混有的水蒸气;吸收鼓入空气中的二氧化碳;
③解:分析坐标,生成二氧化碳的质量为22g,设碳酸氢钠的质量为x,则
2NaHCO3+H2SO4=Na2SO4+2CO2↑+2H2O
168 88
x 22g
$\frac{168}{88}=\frac{x}{22g}$
x=42g
∴NaHCO3%=$\frac{42g}{50g}$×100%=84%
答:试样中碳酸氢钠的质量分数为84%.
点评 本题综合考查了碳酸钠、碳酸氢钠和碳酸氢铵的知识,回答问题时,可以依据课本已有的知识,灵活应用,所以同学们在平时的学习中要加强知识的理解与应用.


科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
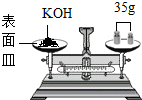 为了除去Na2SO4溶液中的CuSO4杂质,得到纯净的Na2SO4溶液,小王同学做了如下实验:①加入适量的KOH溶液,使CuSO4和KOH恰好完全反应.②过滤,使生成的Cu(OH)2沉淀和液体分离.小王认为得到的无色滤液就是纯净的Na2SO4溶液.请你对小王同学的除杂质实验进行评价:会引入新的杂质硫酸钾
为了除去Na2SO4溶液中的CuSO4杂质,得到纯净的Na2SO4溶液,小王同学做了如下实验:①加入适量的KOH溶液,使CuSO4和KOH恰好完全反应.②过滤,使生成的Cu(OH)2沉淀和液体分离.小王认为得到的无色滤液就是纯净的Na2SO4溶液.请你对小王同学的除杂质实验进行评价:会引入新的杂质硫酸钾查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 原子种类 | 质子数 | 中子数 | 核外电子数 | 核电荷数 |
| A | ||||
| B | 10 | |||
| C | ||||
| D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
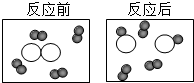 如图是某个化学反应前、后的微观模拟图,请根据图示回答:
如图是某个化学反应前、后的微观模拟图,请根据图示回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | OH -和Cu2+来自同一工厂 | B. | Cu2+和K+来自同一工厂 | ||
| C. | K+和OH -来自同一工厂 | D. | H+和K+ 来自同一工厂 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | I2O7 | B. | I2O3 | C. | I2O4 | D. | I2O5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com