
FeCl3可用作催化剂和外伤止血剂.某实验兴趣小组利用FeCl3腐蚀电路铜板后的溶液(主要成分为FeCl2、CuCl2)进行了氯化铁回收实验.
实验一:(如图1)
(1)写出步骤①中发生的化学方程式 ,此反应的基本类型是 .
(2)步骤②中的操作a名称是 ;步骤③中加入稀盐酸的目的是 .
实验二:该实验小组同学通过查阅资料,又进行了另一种尝试.
【阅读资料】不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离.
如表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
Fe(OH)3 Cu(OH)2
开始沉淀的pH 1.9 4.7
沉淀完全的pH 3.2 6.7
(3)如图2,步骤b加入CuO消耗溶液甲中的HCl,使溶液pH增大到所需范围,请写出盐酸与氧化铜反应的化学方程式 ;你认为步骤b调节溶液的pH到 (数值范围)比较合适.
(4)该实验需要用pH试纸测量溶液的pH,请将pH试纸的使用方法补充完整: ,把试纸显示的颜色与标准比色卡比较,读出该溶液的pH.
(5)FeCl3溶液容易生成Fe(OH)3发生变质,在保存FeCl3溶液时,常向FeCl3溶液中加入某种酸,以防止FeCl3溶液变质,你认为选用 (用字母表示)最合理.
A.稀硝酸 B.稀硫酸 C.稀盐酸 D.稀醋酸.
科目:初中化学 来源: 题型:
根据生活经验和所学知识判断,下列课外实验不能成功的是
A.用pH试纸检验酸牛奶是否变质 B.用肥皂水鉴别硬水和软水
C.用食醋除去暖水瓶中的水垢 D.用紫甘蓝和酒精溶液制酸碱指示剂
查看答案和解析>>
科目:初中化学 来源: 题型:
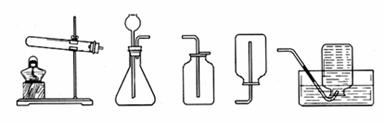 |
A B C D E
(1)实验室要用KClO3和MnO2制取氧气,应选用发生装置是(填编号) ,若用排水法收集氧气,收集完毕后,应先 ,再移开酒精灯。
(2)装满氧气的集气瓶应盖上玻璃片后, (填正放或倒放)在桌面上,其验满的操作方法是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
海洋中蕴含丰富的资源.
(1)海水淡化是解决淡水资源不足的重要方法.下列方法中,可以使海水变为淡水的是 (填字母序号).
A.滤纸过滤 B.吸附 C.沉降 D.蒸馏
(2)从海水中提炼出来的重水(D2O)可作原子能反应堆的中子减速剂和热传热介质.重水中重氢原子(D)的相对原子质量是2,则重水中氢元素的质量分数为 .
(3)从海水中制备纯碱和金属镁的流程如图所示:
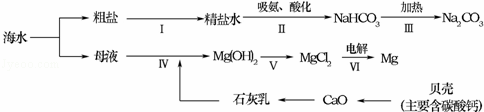
回答下列问题:
①步骤Ⅴ中所加试剂是 .
②粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下了物质,利用过滤等操作进行除杂,则加入下列三种物质的先后顺序为 (填字序号).
a.适量的盐酸 b.稍过量的Na2CO3溶液 c.稍过量的Ba(OH)2溶液
③第Ⅲ歩反应的化学方程式是 .
④在海边用贝壳作原料制生石灰,比用石灰石作原料的优点是 (写一条).
查看答案和解析>>
科目:初中化学 来源: 题型:
南海、钓鱼岛及其附属海域是我国固有领土,蕴藏着丰富的海洋资源.
(1)海水制盐.从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质,为得到较纯的氯化钠,将粗盐溶于水,然后进行如下操作:a.加过量的Ba(OH)2溶液;b.加稍过量的盐酸;c.加过量的Na2CO3溶液;d.过滤;e.蒸发.正确的操作顺序是 (填字母).加Na2CO3溶液的作用是除去 .
(2)海水淡化.如图1是一个简易的蒸馏法淡化海水的装置,证明得到的水是淡水的方法是 .
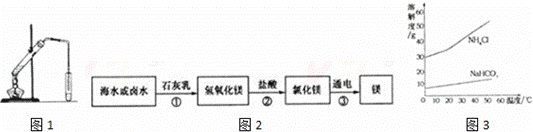
(3)海水制镁.从海水中提取金属镁的过程如图2所示:
在上述转化过程中发生中和反应的是 (填反应顺序号),海水中本身就含有氯化镁,则①、②两步的作用是 .
(4)海水“制碱”.氨碱法制纯碱是先通过化学反应生成NaHCO3和NH4Cl,NaHCO3结晶析出,再加热NaHCO3制得纯碱.
①氨碱法制纯碱中生成NaHCO3和NH4Cl的质量比为84:53.5,NaHCO3和NH4Cl的溶解度曲线如图3所示,请分析NaHCO3结晶析出而NH4Cl没有结晶析出的原因是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
海洋是人类巨大的资源宝库,从海水中提取金属镁的过程如下所示。

请回答:
(1) 在过程①的化学反应中_ _大量的热(填写“放出”或者“吸收”);若在实验室中进行试验,海水和石灰乳充分反应后,操作I的名称是__。
(2) 写出过程③中反应的化学方程式_,过程④中化学反应的基本类型是__ _反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
下列说法中正确的是( )
A.食用“地沟油”对人体有害
B.煤、石油、天然气都属于可再生能源
C.为保障食品安全,杜绝使用任何食品添加剂
D.为提高农作物产量,应大量施用化肥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com