
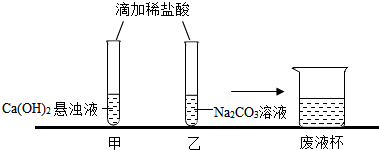
分析 【观察与讨论1】根据氢氧化钙和稀盐酸反应能生成氯化钙和水进行分析;
【观察与讨论2】根据只有当稀盐酸足量时,碳酸钠溶液才能够和稀盐酸反应生成二氧化碳进行分析;
【观察与讨论3】根据无论氢氧化钙和稀盐酸是否恰好完全反应,形成的溶液中一定含有氯化钙进行分析;
根据无论碳酸钠和稀盐酸的质量如何,形成的溶液中一定含有氯化钠进行分析;
【猜想与假设】如果物质之间恰好完全反应时,废液中含有氯化钙和氯化钠;
如果稀盐酸过量时,废液中含有氯化钙、氯化钠和氯化氢;
如果稀盐酸不足,废液中含有碳酸氢钠、氯化钙和氯化钠;
【结论与反思】根据实验现象可以判断废液中溶质的组合情况;
根据氧化铁和稀盐酸反应生成氯化铁和水,氯化铁溶液是黄色的进行分析;
【表达与交流】根据酸性溶液能够腐蚀下水道,需要处理再排放进行分析.
解答 解:【观察与讨论1】盐酸和氢氧化钙反应生成氯化钙和水,所以甲同学在做实验时观察到的明显现象是悬浊液变澄清;
【观察与讨论2】盐酸足量,盐酸和碳酸氢钠反应会生成氯化钠、水和二氧化碳,所以乙同学实验时还应继续加入稀盐酸,才能观察到有气泡产生;
【观察与讨论3】无论氢氧化钙和稀盐酸是否恰好完全反应,形成的溶液中一定含有氯化钙,所以甲同学的试管中废液含有的溶质一定有氯化钙,化学式是CaCl2;
无论碳酸钠和稀盐酸的质量如何,形成的溶液中一定含有氯化钠,所以乙同学的试管中废液含有的溶质一定有氯化钠,化学式是NaCl;
【猜想与假设】
如果物质之间恰好完全反应时,废液中含有氯化钙和氯化钠,所以猜想1:废液中含有CaCl2、NaCl两种溶质;
如果稀盐酸过量时,废液中含有氯化钙、氯化钠和氯化氢,所以猜想2:废液中含有CaCl2、NaCl、HCl三种溶质;
【活动与探究】
甲同学实验:取少量废液于试管中,向其中滴加盐酸,无气泡产生,说明溶液中不含有碳酸氢钠;
乙同学实验:取少量废液于试管中,向其中滴加紫色石蕊试液,溶液变红色,说明溶液中含有氯化氢.
【结论与反思】(1)由以上分析可知,猜想2正确;
(2)要得到相同的结论,还可采用很多种方法,如加入氧化铁粉末,可观察到溶液呈黄色,氧化铁和盐酸反应生成氯化铁和水,化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O;
【表达与交流】若直接排放废液,可能造成的危害是腐蚀下水道等;处理该废液的方法是:将废液中和至中性再排放.
故答案为:【观察与讨论1】悬浊液变澄清;
【观察与讨论2】继续滴加稀盐酸;
【观察与讨论3】CaCl2,NaCl;
【猜想与假设】NaCl、CaCl2,
NaCl、CaCl2、HCl;
【结论与反思】2,黄,Fe2O3+6HCl=2FeCl3+3H2O;
【表达与交流】腐蚀下水道,将废液用熟石灰中和至中性再排放.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.


科目:初中化学 来源: 题型:选择题
| A. | 做化学实验时,取出的多余药品应放回到原试剂瓶中,避免浪费 | |
| B. | 易燃、易爆药品与有强氧化性的物质要分开放置并远离火源 | |
| C. | 不慎将酒精灯碰倒,洒出的酒精在桌上燃烧起来,立刻用湿布扑灭 | |
| D. | 不慎将氢氧化钠溶液沾到皮肤上,立即用大量水冲洗,再涂上硼酸溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
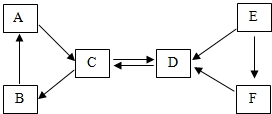 现有A-F六种常见物质,其中B是食品包装中常用的干燥剂氧化钙,A.B、C三种白色固体都含有同种金属元素,E是固体单质,D、E、F都含有同种非金属元素.它们的转化关系如图所示.请回答:
现有A-F六种常见物质,其中B是食品包装中常用的干燥剂氧化钙,A.B、C三种白色固体都含有同种金属元素,E是固体单质,D、E、F都含有同种非金属元素.它们的转化关系如图所示.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
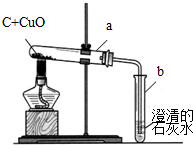 一包黑色粉末可能是由氧化铜和碳粉中的一种或两种物质组成,某学校科学小组为确定其成分,取少量该黑色粉末于烧杯中,加入过量稀硫酸,充分搅拌后观察.下表是实验中可能出现的现象与对应结论,请你填写下表中空白处的相关内容:
一包黑色粉末可能是由氧化铜和碳粉中的一种或两种物质组成,某学校科学小组为确定其成分,取少量该黑色粉末于烧杯中,加入过量稀硫酸,充分搅拌后观察.下表是实验中可能出现的现象与对应结论,请你填写下表中空白处的相关内容:| 现象 | 结论 |
| 溶液呈蓝色,有黑色不溶物 | 含CuO、C |
| 溶液颜色无明显变化,有黑色不溶物 | 只含C |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
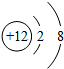 Mg2+.
Mg2+.查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 只有热水的分子在做热运动 | |
| B. | 热水有内能,冷水没有内能 | |
| C. | 温度越高,分子运动越剧烈 | |
| D. | 扩散只能在液体中发生,不能在气体、固体中发生 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 食物腐败--分子本身发生变化 | |
| B. | 酒精挥发--分子间间隔变大 | |
| C. | 热胀冷缩--分子大小随温度变化而改变 | |
| D. | 花香四溢--分子不停地运动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com