
| A. | 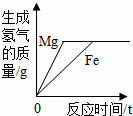 相同质量的镁粉和铁粉分别与过量且溶质质量分数相同的稀硫酸反应 | |
| B. | 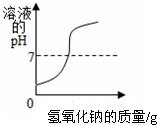 向稀盐酸中滴加过量的氢氧化钠溶液 | |
| C. |  向硝酸铜和硝酸的混合溶液中逐滴加入氢氧化钠溶液 | |
| D. | 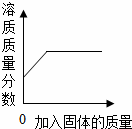 向一定量不饱和的硝酸钾溶液中不断加入硝酸钾晶体(不考虑温度变化) |
分析 根据图中提供的信息可以进行相关方面的判断.
解答 解:A.图示等质量的镁和铁分别加入过量的稀硫酸,生成氢气的质量相等,与反应事实不符,因为等质量的两金属完全反应后,根据反应的化学方程式可知,镁产生氢气质量大于铁,该选项不合理;
B.向稀盐酸中滴加过量的氢氧化钠溶液,随着氢氧化钠的增多,溶液酸性逐渐减小,当盐酸反应完氢氧化钠过量后,溶液显碱性,该选项合理;
C.向硝酸和硝酸铜的混合溶液中加氢氧化钠溶液,氢氧化钠先与硝酸反应生成硝酸钠和水,待硝酸完全反应,再与硝酸铜反应形成氢氧化铜沉淀,至硝酸铜完全反应沉淀质量不再增加,该选项合理;
D.向不饱和溶液硝酸钾溶液中不断加入硝酸钾晶体,溶液中溶质的质量分数增大,当溶液达到饱和状态后,溶质的质量分数不再增大,该选项合理;
故选:A.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 只含有碳、氢、氧元素 | |
| B. | 一定含有碳、氢、铜元素,可能含有氧元素 | |
| C. | 一定含有碳、氢、氧元素,可能含有铜元素 | |
| D. | 肯定含有碳、氢、氧、铜四种元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
①取少量样品溶于水,加入过量的氯化钙溶液 | 有白色沉淀产生 | 该反应的化学方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl |
| ②将上述反应后的混合物过滤,取滤液,加入酚酞试液 | 溶液变红色 | 证明猜想Ⅱ正确 |

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用汽油除去衣服上的油污 | B. | 用水除去衣服上的汗渍 | ||
| C. | 用洗洁精洗碗 | D. | 用酒精将试管壁上的碘洗掉 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水$\stackrel{通电}{→}$氢气+氧气 | |
| B. | 过氧化钠+二氧化碳--碳酸钠+氧气 | |
| C. | 过氧化氢$\stackrel{催化剂}{→}$ 水+氧气 | |
| D. | 高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com