(2013?朝阳区一模)金属结构和性质等是化学研究的重要内容.
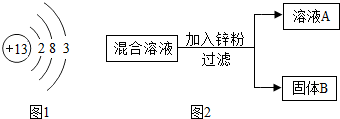
(1)如图1是铝的原子结构示意图.下列说法不正确的是
C
C
.
A.铝原子的质子数为13
B.化合物中铝元素通常显+3价
C.铝是地壳中含量最多的元素
D.铝可作导线是由于它具有良好的导电性
(2)工业上用CO和赤铁矿石炼铁的化学方程式为
.
(3)R是银白色金属,将稀盐酸分别加入到盛有金属Fe、R、Cu的试管中,只有Cu表面无现象;将 FeSO
4溶液中分别加入到盛有金属R、Cu的试管中,只有R表面有黑色物质析出,则金属H、Fe、R、Cu活动性由强到弱的顺序是
R>Fe>H>Cu
R>Fe>H>Cu
.
(4)某化学小组用一定量AgNO
3和Cu(NO
3)
2混合溶液进行了如图2所示实验,下列关于溶液A中的溶质不合理的猜想及其理由是
猜想2,猜想②中无硝酸铜,说明Cu(NO3)2已与锌反应生成Cu,而铜能与硝酸银反应,所以有铜剩余时不可能存在硝酸银.
猜想2,猜想②中无硝酸铜,说明Cu(NO3)2已与锌反应生成Cu,而铜能与硝酸银反应,所以有铜剩余时不可能存在硝酸银.
.
猜想1:只有Zn(NO
3)
2 猜想2:Zn (NO
3)
2、AgNO
3猜想3:Zn (NO
3)
2、Cu(NO
3)
2猜想4:Zn (NO
3)
2、AgNO
3、Cu(NO
3)
2若“猜想1”成立,通过实验确定固体B的成分的方案是
取少量固体B于试管中,加入足量的稀盐酸(或稀硫酸),若有气泡产生则固体B的成分是Zn、Cu、Ag的混合物,若无气泡产生则固体B的成分是Cu、Ag的混合物.
取少量固体B于试管中,加入足量的稀盐酸(或稀硫酸),若有气泡产生则固体B的成分是Zn、Cu、Ag的混合物,若无气泡产生则固体B的成分是Cu、Ag的混合物.
.

 (2013?朝阳区一模)金属结构和性质等是化学研究的重要内容.
(2013?朝阳区一模)金属结构和性质等是化学研究的重要内容.

 (2013?朝阳区一模)某化学小组同学利用如图所示装置进行实验.
(2013?朝阳区一模)某化学小组同学利用如图所示装置进行实验.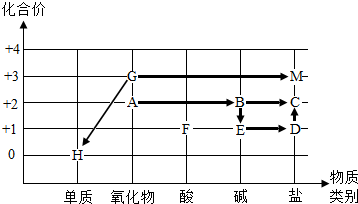 (2013?朝阳区一模)同学们依据物质类别和物质中某种元素的化合价构建了初中化学常见物质间的转化关系坐标图(图中“→”表示物质间的转化).
(2013?朝阳区一模)同学们依据物质类别和物质中某种元素的化合价构建了初中化学常见物质间的转化关系坐标图(图中“→”表示物质间的转化). (2013?朝阳区一模)实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀的质量关系如图所示.
(2013?朝阳区一模)实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀的质量关系如图所示.