
| A. | 氨气是湿润的蓝色石蕊试纸变红 | |
| B. | 细铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成黑色固体 | |
| C. | 加热“铜绿”时,绿色固体变成黑色,管壁出现小水珠 | |
| D. | 向氯化钠溶液中滴加硝酸银溶液,生成白色沉淀 |
分析 A、根据氨水能使红色石蕊试纸变蓝考虑;B、根据铁丝燃烧的现象考虑;C、根据碱式碳酸铜受热分解生成氧化铜、水和二氧化碳考虑实验现象;D、根据氯化钠与硝酸银反应生成氯化银沉淀和硝酸钠考虑.
解答 解:A、氨气溶于水,形成氨水,氨水能使红色石蕊试纸变蓝,故A说法错误;
B、铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成黑色固体,故B说法正确;
C、碱式碳酸铜受热分解生成氧化铜、水和二氧化碳,所以实验现象是:绿色固体变成黑色,管壁出现小水珠,故C说法正确;
D、氯化钠与硝酸银反应生成氯化银沉淀和硝酸钠,所以生成白色沉淀,故D说法正确.
故选A.
点评 实验现象的描述:不能说出生成物名称,通过感官能获取到的信息.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:填空题
 根据下列溶解度表和溶解度曲线回答问题.
根据下列溶解度表和溶解度曲线回答问题.| 温度/℃ | 0 | 20 | 40 | 60 |
| KNO3溶解度/g | 13.3 | 31.6 | 63.9 | 110 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 FeCl3溶液能对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响.
FeCl3溶液能对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响. | 30% H2O2溶液的体积(mL) | 2% FeCl3溶液的体积(mL) | 加入H2O的体积(mL) | 反应的时间(min) | 生成O2的体积(mL) |
| 1 | 5 | x | 20 | 5 | V1 |
| 2 | 10 | 3 | 15 | y | V2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将农田中产生的秸秆就地焚烧 | B. | 将废旧电池深埋 | ||
| C. | 增加植树造林面积 | D. | 高炉炼铁的废气直接排放到大气中 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 有机物:甲烷、二氧化碳 | B. | 盐类:烧碱、纯碱 | ||
| C. | 混合物:自来水、冰水共存物 | D. | 氧化物:水、二氧化锰 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 波尔多液的配制可以在铁质容器中进行 | |
| B. | 铝制品抗腐蚀能力较铁制品强 | |
| C. | 用FeSO4溶液、Cu和Ag三种物质可以验证Fe、Cu、Ag三种金属的活动性强弱顺序 | |
| D. | 铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是Fe3O4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

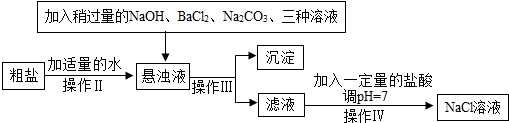
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com