
分析 (1)根据题中的叙述找出反应物、生成物以及反应条件,然后依据质量守恒定律书写化学方程式;
根据增大反应物的接触面积可以加快反应速率进行分析;
(2)根据大量排放出的SO2能形成酸雨,氨水是一种常见的碱分析,根据足量的二氧化硫,与氨水生成亚硫酸铵,不足量的二氧化硫,与氨水反应生成亚硫酸氢铵进行分析;
(3)根据氧化铁与盐酸的反应写出反应的化学方程式,根据硫酸和氧化铁反应会生成硫酸铁进行分析;
(4)根据题中的反应原理找出反应物、生成物以及反应条件,然后依据质量守恒定律书写化学方程式.
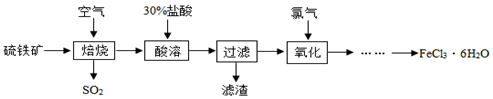
解答 解:(1)硫铁矿和氧气在点燃的条件下生成氧化铁和二氧化硫,化学方程式为:4FeS2+11O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3+8SO2,增大反应物的接触面积可以加快反应速率,所以硫铁矿进行燃烧之前要将其粉碎,增大了反应物的接触面积,其目的是:加快反应速率,使反应更充分;
(2)大量排放出的SO2能形成酸雨,氨水是一种常见的碱,氨水的pH>7,足量的二氧化硫,与氨水生成亚硫酸铵,在农业上可做氮肥;
(3)流程中需用30%的盐酸“酸溶”焙烧后的残渣,盐酸和氧化铁反应生成氯化铁和水,化学方程式为:2Fe2O3+6HCl═2FeCl3+3H2O,酸溶”时可改用硫酸,硫酸和氧化铁反应生成硫酸铁和水,而题中需要制备氯化铁晶体,所以不能改用硫酸,原因是:主产物不再是氯化铁;
(4)通过分析题中的反应原理,酸溶后的混合物中通入氯气制取氯化铁,氯气和氯化亚铁反应生成氯化铁,化学方程式为:2FeCl2+Cl2═2FeCl3.
故答案为:(1)4FeS2+11O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3+8SO2,加快反应速率,使反应更充分;
(2)酸雨,>,氮;
(3)Fe2O3+6HCl=2FeCl3+3H2O,不可以,反应后不能生成FeCl3;玻璃棒,量筒;
(4)2FeCl2+Cl2=3FeCl3.
点评 在解此类题时,首先分析题中的反应原理,然后找出对应的学过的知识点,然后结合题中所给的知识进行分析解答.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
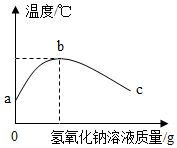 某化学兴趣小组探究硫酸和氢氧化钠中和反应时,利用数字化温度传感器 如图所示的实验图,请据图分析,下列结论正确的是( )
某化学兴趣小组探究硫酸和氢氧化钠中和反应时,利用数字化温度传感器 如图所示的实验图,请据图分析,下列结论正确的是( )| A. | 从图线可知中和反应是先放热后吸热 | |
| B. | 在实验过程中a-b的pH增大,b-c的pH减小 | |
| C. | c点时的溶质为H2SO4和Na2SO4 | |
| D. | b点时向溶液中加入酚酞试液,溶液不变色 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
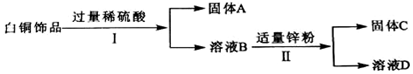
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
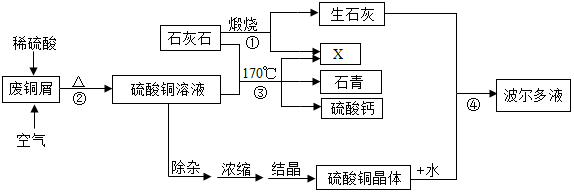
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| 溶解度/g | 14.3 | 17.4 | 20.7 | 25.0 | 28.5 | 33.3 | 40.0 | 55.0 | 75.4 |
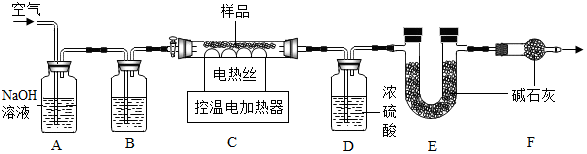
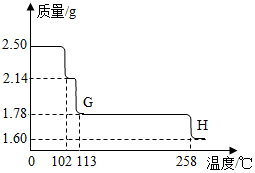
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 若两个粒子核外电子数相同,则一定属于同种元素 | |
| B. | 同种元素组成的物质,一定是单质 | |
| C. | 金刚石和石墨物理性质存在较大差异是由于碳原子排列方式不同 | |
| D. | 硝酸铵固体溶于水放出热量,天然气燃烧吸收热量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com